【JIOHS】【封面文章】ID-OCTA:联合SNR倒数与去相关特征的光学相干血流造影
本文介绍的是浙江大学光电科学与工程学院李鹏副教授课题组对OCTA算法及其应用进行的系统性综述,发表在《Journal of Innovative Optical Health Sciences》期刊2021年第1期。
ID-OCTA: OCT angiography based on inverse SNR and decorrelation features
Huakun Li, Kaiyuan Liu, Lin Yao, Xiaofeng Deng, Ziyi Zhang and Peng Li
研究背景
光学相干层析成像(opticalcoherencetomography, OCT)技术基于光学低相干干涉原理,能够实现生物组织内部非侵入式、实时、高分辨率的结构成像。凭借其“光学切片”的能力,OCT技术已经发展为一种重要的生物医学成像技术。
作为OCT的一种功能成像手段,光学相干血流造影(OCTangiography, OCTA)技术利用血红细胞作为内源性运动对比机制,实现了毛细血管水平快速的三维血流造影。由于其非侵入、非接触以及无标记成像的优势,OCTA技术已经被广泛用于包括眼科、皮肤科、神经科学等领域的临床诊断及科学研究。自从OCTA技术第一次被用于探测血流(基于多普勒原理),为了提高血流造影的灵敏度和对比度,研究人员提出了大量的OCTA算法。
内容简介
本文对OCTA算法及其应用进行了系统性的综述,主要包括基于随机矢量和模型的无标记血流造影运动对比机制,基于信噪比倒数-去相关系数(inverse SNR-decorrelation, ID)特征空间的信噪比自适应ID-OCTA算法,基于Hessian矩阵分析的形态滤波器,采用自适应时空(spatio-temporal, ST)核的定量OCTA算法以及OCTA技术的应用。这些研究对于提高OCTA技术的性能,拓展其在科学研究及临床诊断中的应用具有重要意义。
图文导读
1.复数去相关
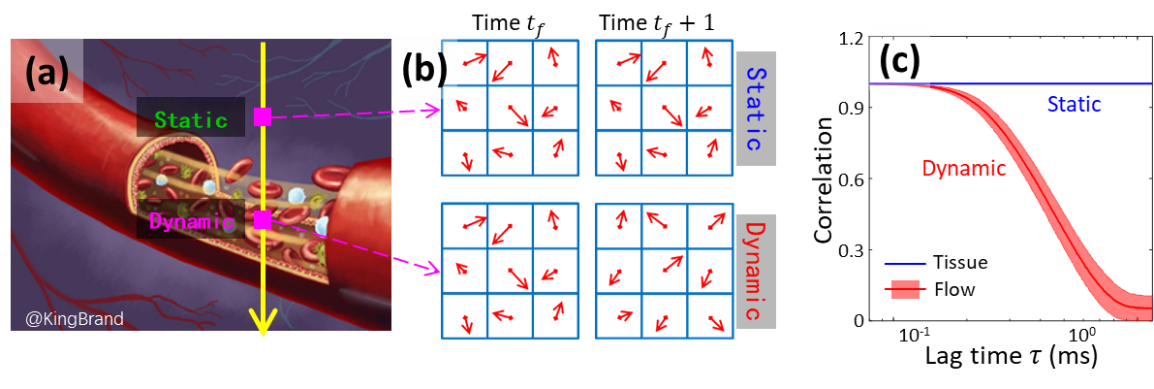
图1:复数去相关计算原理图。(a)血管及周围的静态组织。(b)相邻帧动态血流区域和静态组织区域的OCT信号。(c)动态区域及静态区域相关系数随着去相关计算延迟时间的变化。
动态血流区域的OCT信号随时间改变,而静态组织区域的信号保持稳定。因此,通过计算相同位置不同时间点采集到的OCT信号的相关性,动态血流显示出低相干性(或者高去相关值),而静态组织显示出高相干性(或低去相关值),基于此能够区分动静态信号。
2.ID-OCTA算法
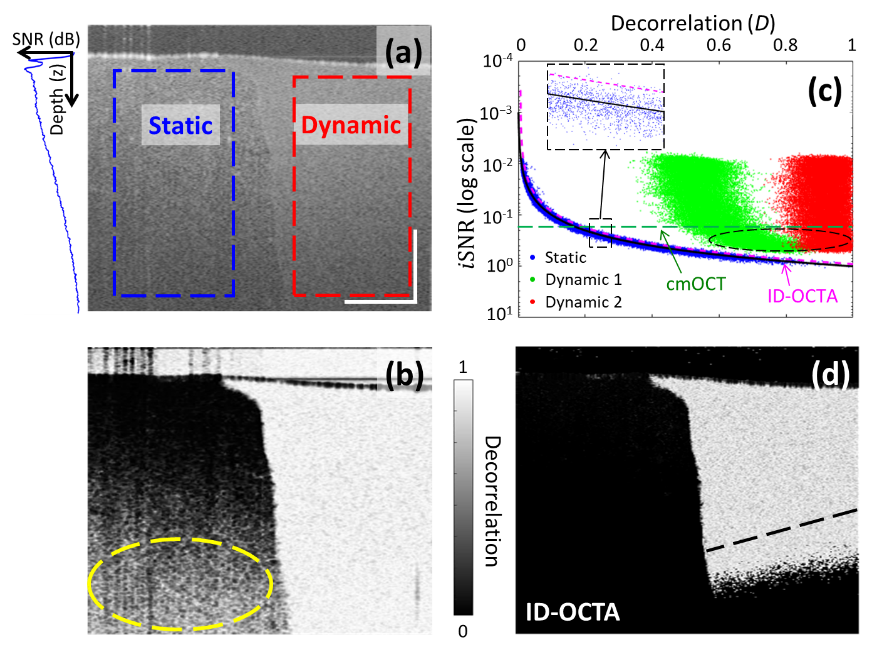
图2:采用流体样品数据验证ID-OCTA算法的有效性。(a)流体样品的结构断层图,左半部分为静态区域,右半部分为动态区域。虚线框表示映射到ID空间的区域。左侧插入图说明信噪比随着深度衰减。(b)去相关值断面图。(c)流体样品数据及提出的ID-OCTA分类器在ID空间的映射结果。静态和噪声信号用蓝色散点标记,不同扫描时间间隔的动态信号用红色(9.9ms)和绿色(3.3ms)的散点标记。对应的理论渐近关系用黑色实线表示,ID-OCTA分类器阈值用品红色虚线表示,cmOCT中的阈值用绿色虚线表示。椭圆框圈出的区域表示被cmOCT去除的动态信号。(d)ID-OCTA算法得到的血流造影断面图,黑色虚线表示cmOCT得到的动态区域边界。
如图2(b),总体来说动态区域呈现出更大的去相关值,静态区域的去相关值更小。然而由于随机噪声的影响,深处的静态区域也展现出高去相关值。图2(c)呈现了动静态信号在ID空间的分布,静态和噪声信号分布在理论的ID渐近线周围(图2(c)中黑色实线)并且可以有效地被ID-OCTA分类器确定的阈值(图2(c)中品红色虚线)去除。作为对比,在correlationmappingOCT(cmOCT)中,一个全局的强度阈值(图2(c)中绿色虚线)被用于去除低信噪比的信号。因此,相较cmOCT,ID-OCTA提高了低信噪比区域动态信号的可见度。
3.形态滤波器
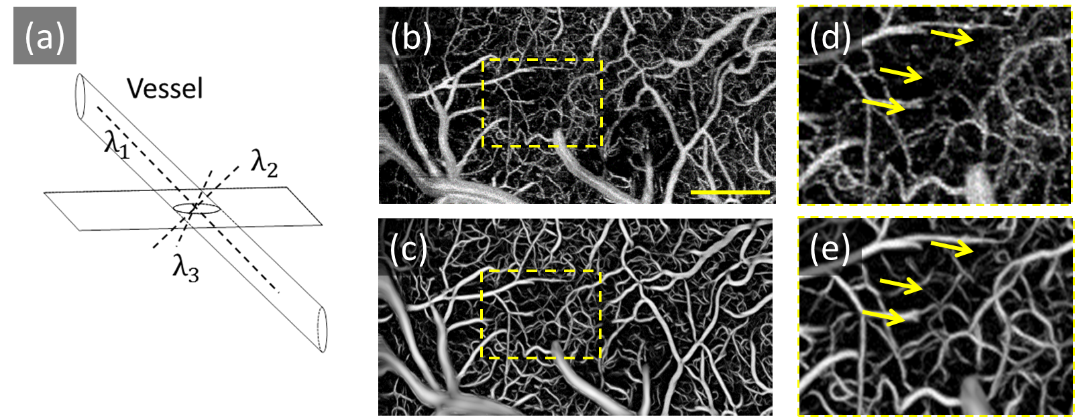
图3:血管形状示意图及三维Hessian滤波器的效果。(a)理想的血管展现出连续的管状结构。Hessian滤波前(b)和滤波后(c)的血流造影投影图。(d)和(e)为图(b)和(c)对应虚线框的局部放大图。比例尺为400μm。
在原始的血流造影投影图中(图3(b)、3(d)),存在大量的噪声,而基于三维Hessian矩阵分析的形态滤波器显著改善了血流对比度和血管的连续性(图3(c)、3(e))。
4.大鼠脑中风模型研究
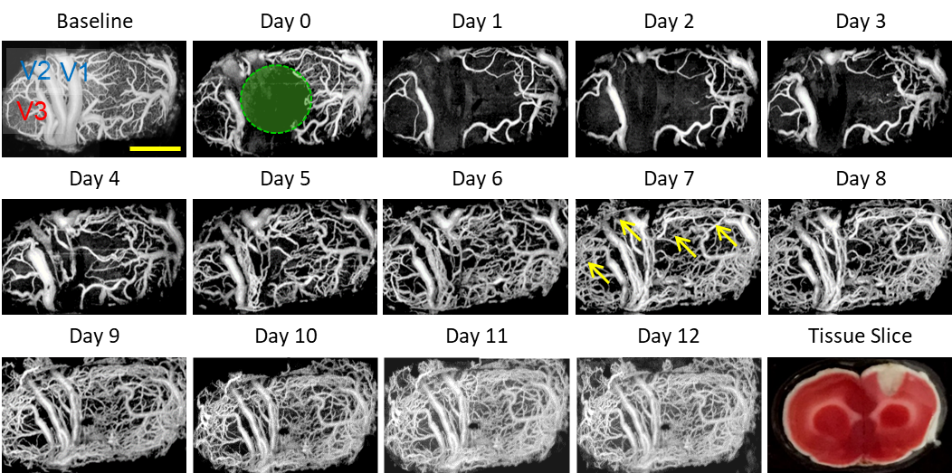
图4:大鼠脑血管缺血性中风模型的长期OCTA成像监测。Baseline和day1分别代表光血栓前以及光血栓形成当日的投影图。绿色圆圈表示激光照射30min的区域。右下角为第一天典型的组织切片。比例尺为1mm。
在光血栓阻塞形成前,大脑中动脉远端、脑膜微血管及皮层毛细血管都清晰可见,在第一天(光血栓形成后1h),局部缺血区域的血流信号全部消失。在之后的三天,伴随着辐射区域以外毛细血管的消失,局部缺血区域显著扩大,而周围区域的大血管的结构保持不变但是直径扩大。从第五天开始,缺血区域和周边区域出现大量的新血管。OCTA技术能够准确评估恢复期血流灌注的时空动态变化,对了解这些血管疾病的病理特征有重要意义。
5.小鼠视网膜成像

图5:小鼠视网膜的ID-OCTA造影结果。(a)~(e)分别为视网膜全层(深度采用颜色编码),浅层血管丛(superficial vascular plexus, SVP),中层血管丛(intermediate vascular plexus, IVP)以及深层血管丛(deep vascular plexus, DVP)和脉络膜的血管造影投影图。比例尺为0.5mm。
实验室系统采用的谱域OCT系统中心波长为840nm,线扫描速率为120kHz。512个A扫描组成一个B扫描,从512个断层位置采集到的1536个B扫描帧(每个位置重复3次),对应的采集时间为6.6s。
6.血液动力学响应研究
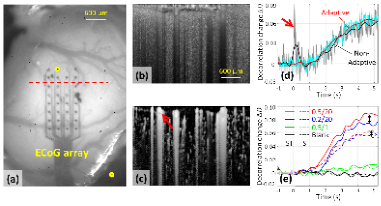
图6:刺激引起的大鼠大脑皮层血液动力学响应。(a)大鼠大脑皮层和透明的皮层电极阵列的照片,黄色圆点为激活的电极。红色虚线表示OCT的B-扫描位置。(b)以去相关系数为对比度的断层图像。(c)以强度加权的去相关系数作为对比度的ID-OCTA断层图像。(d)采用不同设置时对刺激(0.5mA/20pulses)的血液动力学响应:采用固定大小ST核,在EMD滤波前(灰色)及滤波后(黑色),采用自适应ST核,在EMD滤波器前(青色)及滤波后(红色)。血液动力学信号在整个B扫描帧上平均(图6(c)中所有的血管)。(e)采用spatio(S,虚线)核和自适应ST核(实线),对不同刺激(红色:0.5mA/20pulses,蓝色:0.2mA/20pulses,绿色:0.5mA/1pulse,黑色:空白)的血液动力学响应。对单根血管进行平均运算(图6(c)中红色箭头所示)。对所有曲线进行EMD滤波。
通过减去基准状态下的去相关值,刺激引起的血液动力学响应以去相关值的变化来呈现。对比图6(d)中未经滤波的原始曲线(青色和灰色实线),采用自适应大小的ST核(青色)在不改变曲线的整体形状的情况下,有效地抑制了意外的运动伪像(图6(d)中红色箭头处)和高频的波动。此外,如图9(e)所示,自适应大小的ST核相较S核有更大的动态范围,同时提高了不同刺激的区分度。
PI简介
李鹏,浙江大学光电科学与工程学院副教授,博士生导师。长期从事光学相干成像技术及应用研究,发展了运动/光强/图形多维特征空间OCTA等系列技术。在IEEE TMI、JCBFM、OL、BOE等期刊发表SCI论文60余篇。获得浙江省杰出青年基金资助、华为等企业资助,主持各类国家、省部级项目6项。申请/授权国际国内发明专利20余件,实现专利成果医疗产业转化1件。


