偏振空间频域成像系统及仿体验证  下载: 559次
下载: 559次
The Muller matrix, as a method for characterizing the polarization properties of samples, contains complete information about the polarization properties of samples, and it has become an important indicator for characterizing pathological tissues in basic and preclinical studies. However, in the traditional polarized light imaging method for measuring the Muller matrix, the scattering depth of polarized light in collagen tissue cannot be controlled. The obtained Muller matrix information is the average of unknown depths in collagen tissue, and it is impossible to accurately measure the Muller matrix information of the pathological tissue area. Polarized spatial frequency domain imaging (PSFDI), which combines spatial frequency domain imaging (SFDI) and polarized light imaging, is applied to measure the optical properties of biological tissues accurately.
SFDI relates the spatial frequency of the projected stripe pattern to the penetration depth of the detected light, and the imaging depth can be controlled by controlling the spatial frequency of the projected light. We designed and validated a polarization SFDI system that uses the SFDI technique to control the imaging depth, projects the streak pattern onto the surface of the measured tissue, constructs a polarizer and detector to modulate the polarization state of the polarized light, and then acquires the image data using a CMOS camera and calculates the Mueller matrix information.
Experimental results showed that the grey-scale plate diffuse reflectance measured by the polarization SFDI system was linearly correlated with the standard value (R2=0.99988). The depolarization coefficient tends to be proportional to the fat emulsion volume fraction, the two-way attenuation coefficient increases with the increase of two-way attenuation owing to the two-way attenuator, and the accurate measurement of the phase delay of the quarter-wave and full-wave plates indicates that the system can accurately measure the sample polarization parameters. A comparison of uniform light field illumination and polarization-sensitive SFDI shows that the latter effectively controls the depth and accurately measures the shallow Mueller matrix of the sample. The results of this study are expected to effectively improve the accuracy of the detection of polarization characteristics of superficial tissues and promote early tumor detection.
In this study, a PSFDI system is developed based on polarized light imaging and SFDI, and the device structure, measurement method, and data processing method are introduced. By performing the error calibration of the PSFDI device, the measurement error of the device can be less than 2%. By performing Mueller matrix imaging on tissues, we verified the reliability of the device to measure tissue polarization Mueller and the accuracy of the Mueller matrix decomposition; hence, PSFDI can be used to obtain the optical properties of various samples. The PSFDI can accurately image pathological regions, providing accurate physiological parameters for pathological analysis, and it has a wide range of biomedical applications.
1 引言
穆勒矩阵可以完全表征样品的偏振属性,含有反映样品偏振特性的完整信息,已成为基础和临床前研究中表征病变组织的重要指标,近年来已被广泛应用于胶原纤维[1-2]、烧伤创面[3-4]、癌症组织[5-6]检测等领域。穆勒矩阵携带的组织相关信息(如透射、反射、二向衰减、相位延迟、退偏等)对于分析生物组织病变信息具有重要帮助。例如,病理组织(例如癌变组织)因为高度组织化的显微结构被破坏而丧失了组织形态的固有异质性,从而能更好地保留探测光的偏振状态,具有更低的退偏特性。瘢痕组织含有密集的胶原纤维,探测光束在该组织样本中传播时会发生更多的正交偏振态相移,从而具有高线性延迟性[7]。生物组织基质的异常改变(例如胶原蛋白的重塑)会导致组织的散射和吸收特性发生改变,从而使得组织的去偏振特性发生改变[8]。
偏振光成像具有宽场、无创、定量检测等优点,长期以来被应用于生物组织穆勒矩阵的测量。Azzam[9]在1978年提出的波片旋转法中详细介绍了穆勒矩阵的求解,此后该方法在穆勒矩阵的测量中得到了广泛应用[6,10-11],其测量装置主要由光源、偏振片、四分之一波片、工业CCD相机组成。在测量过程中,光源产生的入射光经由偏振片和四分之一波片构成的起偏器(PSG)后被调制为不同的偏振态,接着入射至待测样品组织,经样品组织散射后,不同偏振态的散射光经检偏器(PSA)调制偏振态后被CMOS相机捕捉。成像图片的像素值为散射光的光强值,以时间和光强值为轴绘制曲线,所得曲线为周期曲线。应用离散傅里叶变换求解离散傅里叶级数,然后根据对应关系即可求解出穆勒矩阵。2002年,Baba等[12]对实验装置进行了改进,用偏振片、电动偏振旋转器、可变延迟器构成新的起偏器与检偏器。在测量过程中,光源产生的入射光经起偏器调制为特定的偏振态并入射至待测样品组织,经样品组织散射的特定偏振态的散射光由检偏器调制成同一偏振态并被CMOS相机捕捉,由不同偏振态的散射光光强即可计算得到样品组织的穆勒矩阵。也有其他简化或提高测量精度的改进措施,如:Anastasiadou等[13]用4个液晶相位延迟器替换电动偏振旋转器和可变延迟器,构成了新的起偏器和检偏器。目前,已有不同的穆勒矩阵计算方法,如基于基尔霍夫近似方法的穆勒矩阵测量法[14]和基于邦加球轨迹的穆勒矩阵测量法[15]。
在传统的偏振光成像方法中,偏振光在生物组织中的散射深度无法控制,所求穆勒矩阵是生物组织未知深度处穆勒矩阵的平均值,无法精确测量病理组织区域的穆勒矩阵信息。以皮肤疾病为例,大多数病理组织区域位于皮肤浅层,对于传统的偏振光成像来说,偏振光的穿透深度大于病理组织的深度,所求穆勒矩阵不够准确,不具有医学参考价值。这里以穆勒矩阵中的退偏系数为例进行说明,分子与光子间的碰撞会改变光子的偏振态,随着碰撞事件增多,光子的偏振态改变,相应表现为退偏系数增大。传统的偏振光成像方法无法控制成像深度,因此,在不同的光照条件下(即入射光穿透深度不同),求得的退偏信息也不相同。
近年来,结合空间频域成像(SFDI)和偏振光成像的偏振空间频域成像(PSFDI)技术被广泛用于准确测量生物组织的光学特性。Yang等[16]设计了一套偏振空间频域系统装置,并用其检测了牛肌腱组织的纤维方向,取得了良好的实验结果。Jett等[17]利用偏振空间频域成像技术对二尖瓣叶组织胶原在机械负载下的纤维排列进行了定量分析,并粗略计算出了该组织的穆勒矩阵信息。空间频域成像将投射条纹图案的空间频率fx与探测光的穿透深度联系起来,通过控制投射光的空间频率fx来控制成像深度,有效解决了传统偏振光成像的缺陷,使得病理组织区域穆勒矩阵的测量具有可行性。本团队设计了一套偏振空间频域成像系统,使用QT平台编写的控制软件对其进行控制。该系统可以同时对组织切片和活体胶原组织进行快速测量。此外,本团队设计了MATLAB算法,用于计算并验证所测胶原组织的穆勒矩阵信息,同时对穆勒矩阵进行了分解,以求解该胶原组织的相关光学特性。
2 原理与方法
2.1 偏振空间频域成像系统
如
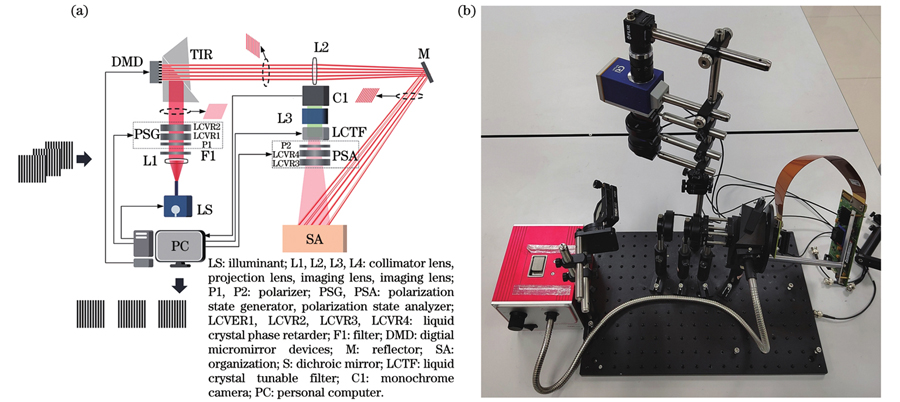
图 1. 偏振空间频域成像系统。(a)原理图;(b)实物图
Fig. 1. Polarization spatial frequency domain imaging system. (a) Schematic; (b) physical drawing
2.2 穆勒矩阵和极化分解
使用斯托克斯矢量来定义光的偏振状态,并使用穆勒矩阵来描述结构光通过系统时偏振态的变化。斯托克斯矢量表达式为
式中:S1表示总光强,即水平偏振分量与垂直偏振分量之和;S2表示水平偏振分量与垂直偏振分量之差;S3表示45°偏振分量与135°偏振分量之差;S4表示右旋圆偏振分量与左旋圆偏振分量之差。通过
穆勒矩阵中的每一个元素分别表征被测样品的一种偏振信息,当被测样品仅表现出单一光学性质时,根据元素的对应位置可以得到穆勒矩阵含有的偏振信息。但当一个样品表现出混合光学性质时,穆勒矩阵的元素混合在一起,导致解释变得复杂。此时需要将混合穆勒矩阵分解为多个代表单一光学性质的穆勒矩阵[18]。目前广泛使用的是Lu和Chipman[19]提出的极化分解方法。此方法依据偏振介质传输的三个特性[二向色性(与偏振有关的强度衰减性质)、相位延迟(与偏振有关的相位改变性质)和散射退偏(偏振光转化为非偏振光的性质)]将穆勒矩阵分解为三个因子的乘积,分解得到的子矩阵能够独立体现介质的偏振特性。数学公式为
式中:
式中:
2.3 空间频域成像
空间频域成像具有宽场、无创、定量检测等优点,能够在实现组织形态结构检测的同时,提供组织的光学、生理参数信息,近几年来常被用于生物组织的生理特征测量,可为临床检测提供相关数据[20-21]。空间频域成像基于宽场光源和空间光调制器,结合光传输模型来量化组织的光学属性,可以更好地量化组织中各成分的生理属性。
空间频域成像使用一个数字微镜芯片烧录不同空间频率fx的明暗条纹图案(一般为3张,空间相位间隔120°),结构光入射至烧录条纹图案的DMD后被投影在待测组织上,结构光在样品表层组织中发生散射,散射光被探测相机接收后输出,共获得3张光强图片(一般记录为I0、I120、I240)。结构光的总光照强度I被分解为直流DC(样品在平面照明下的反射分量)和交流AC(在给定空间频率下解调的反射分量)两部分,这两部分的数学公式(三相位移法)为
实验证明,随着空间频率fx增大,交流分量减小,因此限制了结构光在待测组织中的散射深度[22]。可以通过控制投射条纹图案的空间频率来控制采样深度,使采样深度限制在病理区域。在低空间频率下,有效采样深度d的计算公式为
式中:
2.4 偏振空间频域成像
在偏振空间频域成像测量开始之前,先基于空间频域成像原理计算出生物组织的吸收系数和散射系数,详细的计算过程可参考Cuccia等[21]的论文;然后计算0.5 cm成像深度下条纹图案的空间频率,并使用该条纹图案进行投射测量。在测量过程中,调制起偏器和检偏器的偏振态分别为水平线偏振态(H)、垂直线偏振态(V)、45°线偏振态(P)和右旋圆偏振态(R)。起偏器和检偏器两两组合共有16种偏振态组合,在每一种组合下对样品进行测量。投射的条纹图案共有3张,即每一种组合测量生成3张图像,16种组合共计生成48张图像。在偏振空间频域成像测试之后,对每一种偏振态组合下的3张图像使用三相位移法(使用AC分量)求得一张完整的偏振光图像,共获得16张完整的偏振光图像,然后求解生物组织的穆勒矩阵
其中,
设计相关实验,对求解穆勒矩阵的正确性进行验证。求得生物组织的穆勒矩阵后,对穆勒矩阵进行极化分解(分解算法使用MATLAB编写而成),并根据样品的偏振光学特征分析其生物特征。关于穆勒矩阵分解的正确性,也须设计相关实验进行验证。
3 结果与讨论
3.1 穆勒矩阵验证实验
使用已知穆勒矩阵的物品进行测量,并将测量值与实际值进行比较,以验证偏振空间频域成像系统的准确性。为此,使用梯度漫反射板进行实验。在漫反射板实验中,所用漫反射板的漫反射率分别2%、5%、10%、20%、40%、60%、80%、99%。因为漫反射板的归一化穆勒矩阵恒为
无法比较不同漫反射板之间的差别,因此使用未归一化的穆勒矩阵进行比较。在未归一化的穆勒矩阵中,m11的大小反映的是漫反射板反射率的大小。
开始测量之前,需要对系统进行标定。通过对白板(即100%漫反射率的漫反射板)进行多次测量,计算穆勒矩阵中每一个元素值的归一化均值来统计误差。均值穆勒矩阵为
可以看出,实验测量结果符合漫反射板的穆勒矩阵形式。在之后的梯度漫反射板穆勒矩阵的计算中会减去各个位置上的误差,以便使测量结果更为精确。
对于不同反射率的漫反射板使用不同的曝光时间,以便使测量图像具有更高的灰度值。最后统计数据,对曝光时间进行归一化,计算相同曝光时间下梯度漫反射板的穆勒矩阵信息,并将矩阵中的m11值除以标定情况下白板的m11值,观察m11值与反射率之间的关系。如

图 3. m11值与梯度漫反射板反射率的关系
Fig. 3. Relationship between m11 and reflectance of gradient diffuse reflector
3.2 穆勒矩阵极性分解验证实验
穆勒矩阵可分解为3个矩阵,这3个矩阵分别可表示为衰减器、延迟器和去偏器。验证实验步骤如下:用实际的装置或器材分别单独代表3个分类,然后通过控制变量法,改变其中的一个变量,观察对应的矩阵及参数变化。分解实验验证示意图如
第一个样品为脂肪乳溶液,代表去偏器。偏振光入射脂肪乳溶液后发生散射,仅改变偏振光的偏振方向,不改变光通量和光的相位延迟。这种混浊介质的归一化穆勒矩阵的一般形式为对角去偏器,即
式中:dl表示混浊介质对线偏振光的转换能力;dc表示圆偏振光的转换能力。
第二个样品为两块折射率为1.5的玻璃片,代表衰减器。偏振光入射至玻璃表面时的光强、反射率与入射角及偏振光的偏振态有关,即:对于不同偏振态的偏振光,通过固定角度的玻璃后,其光强不一致。所以,本文选用玻璃片来模拟二向衰减特性。实验所用玻璃片的直径为25.4 mm,可覆盖相机的拍摄范围,而且玻璃片由光学支架固定,可以自由移除和插入。
第三个样品为波片,代表延迟器。使用不同相位延迟的波片(全波片和四分之一波片)进行实验,用以验证装置的准确性。波片同样由光学支架固定,可以自由移除和插入。
实验分为三组,第一组为梯度脂肪乳溶液实验。在此实验中,通过改变脂肪乳溶液的体积分数来观察退偏系数是否具有增长趋势以及衰减系数和相位延迟是否保持不变。梯度脂肪乳溶液实验参数设置如
表 1. 梯度脂肪乳溶液实验参数设置
Table 1. Parameter setting in gradient fat emulsion solution experiment
|
第二组为梯度玻璃片角度实验,其中,玻璃片角度为两块玻璃片与水平面夹角之和。在此实验中,通过改变玻璃片角度来观察衰减系数是否具有增长趋势以及退偏系数和相位延迟是否保持不变。梯度玻璃片角度实验参数设置如
表 2. 梯度玻璃片角度实验参数设置
Table 2. Parameter setting in gradient glass sheet angle test
|
第三组实验在第一组实验的基础上改用全波片进行测量,并将测量结果与使用四分之一波片的测量结果进行比较。实验结果如

图 5. 极化分解验证实验结果。(a)梯度脂肪乳溶液实验结果;(b)梯度玻璃片角度实验结果;(c)全波片与四分之一波片对比实验结果
Fig. 5. Polarization decomposition validation test results. (a) Experimental results of gradient fat emulsion solution; (b) experimental results of gradient glass sheet angle; (c) comparative experimental results of full wave plate and quarter wave plate
保持玻璃片角度和四分之一波片不变,仅改变脂肪乳溶液的体积分数,实验结果如
实验结果显示,改变某一变量,偏振空间频域成像系统均能检测到对应参数的变化,证明了极化分解的正确性。
3.3 偏振空间频域成像实验
上述实验验证了偏振空间频域成像实验装置及极性分解算法的正确性。基于此,使用偏振空间频域成像方法测量脂肪乳溶液的穆勒矩阵,并将测量结果与传统偏振光成像测量结果进行对比,以验证偏振空间频域成像对深度的控制能力。
配制梯度脂肪乳溶液,观察偏振空间频域成像与传统偏振光成像测量所得退偏系数的变化。共进行两组实验,第一组实验在脂肪乳溶液底部放置反射率为0%的漫反射板,第二组实验在脂肪乳溶液底部放置反射率为100%的漫反射板。
如

图 6. 偏振空间频域成像与传统偏振光成像实验结果。(a)在脂肪乳溶液底部放置0%漫反射板的实验结果;(b)在溶液底部放置100%漫反射板的实验结果
Fig. 6. Experimental results of polarization spatial frequency domain imaging and traditional polarized light imaging. (a) Experimental results for placing diffuse reflection plate with 0% reflectance at the bottom of fat emulsion solution; (b) experimental results for placing diffuse reflection plate with 100% reflectance at the bottom of fat emulsion solution
3.4 烧伤检测
为了验证该实验装置对生物组织测量的正确性,选用新鲜猪皮测量烧伤情况下偏振参数的变化。使用恒温加热平台对猪皮进行加热,以模拟烧伤。在此实验中,猪皮每加热1 min进行一次测量。
与仿体实验不同,在生物组织实验中,入射光入射至皮肤表面发生漫反射,会对偏振光产生去极化影响。为得到精确的测量结果,须排除漫反射的影响。文献[20]详细介绍了生物组织漫反射率的计算方法。在频域中,反射光子密度振幅MAC与调制传递函数fMTF、样品漫反射率Rd、光源强度I0有关,具体关系为
每次测量前计算皮肤的漫反射率,去除皮肤表面漫反射影响后的猪皮烧伤测量结果如

图 7. 烧伤实验结果。(a)猪皮烧伤照片,按加热时间排序;(b)退偏系数与衰减系数曲线图;(c)相位延迟曲线图
Fig. 7. Burn test results. (a) Burn photos of pigskin, sorted by heating time; (b) curves of depolarization coefficient and diattenuation coefficient; (c) phase delay curve
4 结论
本文基于偏振光成像和偏振空间频域成像发展了一种偏振空间频域成像装置,并介绍了装置结构以及测量方法和数据处理方法。对偏振空间频域成像装置进行误差校准,装置的测量误差可低至2%以下。通过对组织等进行穆勒矩阵成像,验证了装置测量组织穆勒矩阵的可靠性以及对穆勒矩阵分解的准确性。目前可以通过偏振空间频域成像获取多种样品的光学特性。与传统的通过偏振光成像求解穆勒矩阵的方法相比,所提方法创造性地引入了空间频域成像技术。在传统的偏振光成像中,偏振光入射至生物组织中的深度无法控制,所求得的穆勒矩阵是生物组织未知深度处的平均值,医学参考意义较小。所提技术通过引入空间频域成像技术来控制成像深度,求得的是生物组织表层已知深度处穆勒矩阵的均值,具有可以精确成像病理区域的能力,可为病理分析提供更精确的生理参数分析,具有广阔的生物医学应用前景。
[1] Goth W, Potter S, Allen A C B, et al. Non-destructive reflectance mapping of collagen fiber alignment in heart valve leaflets[J]. Annals of Biomedical Engineering, 2019, 47(5): 1250-1264.
[2] Ellingsen P G, Aas L M S, Hagen V S, et al. Mueller matrix three-dimensional directional imaging of collagen fibers[J]. Journal of Biomedical Optics, 2014, 19(2): 026002.
[3] Boulvert F, Boulbry B, Le Brun G, et al. Analysis of the depolarizing properties of irradiated pig skin[J]. Journal of Optics A: Pure and Applied Optics, 2005, 7(1): 21-28.
[4] Jiao S L, Yu W R, Stoica G, et al. Contrast mechanisms in polarization-sensitive Mueller-matrix optical coherence tomography and application in burn imaging[J]. Applied Optics, 2003, 42(25): 5191-5197.
[5] Ahmad I, Ahmad M, Khan K, et al. Ex vivo characterization of normal and adenocarcinoma colon samples by Mueller matrix polarimetry[J]. Journal of Biomedical Optics, 2015, 20(5): 056012.
[6] Du E, He H H, Zeng N, et al. Mueller matrix polarimetry for differentiating characteristic features of cancerous tissues[J]. Journal of Biomedical Optics, 2014, 19(7): 076013.
[7] Ahmad I, Khaliq A, Iqbal M, et al. Mueller matrix polarimetry for characterization of skin tissue samples: a review[J]. Photodiagnosis and Photodynamic Therapy, 2020, 30: 101708.
[8] Bartlett M, Huang G, Larcom L, et al. Measurement of particle size distribution in mammalian cells in vitro by use of polarized light spectroscopy[J]. Applied Optics, 2004, 43(6): 1296-1307.
[9] Azzam R M. Photopolarimetric measurement of the Mueller matrix by Fourier analysis of a single detected signal[J]. Optics Letters, 1978, 2(6): 148.
[10] Ye C. Photopolarimetric measurement of single, intact pulp fibers by Mueller matrix imaging polarimetry[J]. Applied Optics, 1999, 38(10): 1975-1985.
[11] 郑州, 侯俊峰. 单波长中红外穆勒矩阵椭偏仪的设计、定标与测试[J]. 光学学报, 2022, 42(18): 1812004.
[12] Baba J S, Chung J R, DeLaughter A H, et al. Development and calibration of an automated Mueller matrix polarization imaging system[J]. Journal of Biomedical Optics, 2002, 7(3): 341-349.
[13] Anastasiadou M, Hatit S B, Ossikovski R, et al. Experimental validation of the reverse polar decomposition of depolarizing Mueller matrices[J]. Journal of the European Optical Society: Rapid Publications, 2007, 2: 07018.
[14] 闫振纲, 孙卫平, 李杰, 等. 基于穆勒矩阵的金属和电介质识别方法[J]. 激光与光电子学进展, 2019, 56(14): 142401.
[15] 肖悦娱, 蒋晓勇, 陈华. 基于邦加球轨迹的穆勒矩阵测量法[J]. 激光与光电子学进展, 2018, 55(12): 122603.
[16] Yang B, Lesicko J, Sharma M, et al. Polarized light spatial frequency domain imaging for non-destructive quantification of soft tissue fibrous structures[J]. Biomedical Optics Express, 2015, 6(4): 1520-1533.
[17] Jett S V, Hudson L T, Baumwart R, et al. Integration of polarized spatial frequency domain imaging (pSFDI) with a biaxial mechanical testing system for quantification of load-dependent collagen architecture in soft collagenous tissues[J]. Acta Biomaterialia, 2020, 102: 149-168.
[19] Lu S Y, Chipman R A. Interpretation of Mueller matrices based on polar decomposition[J]. Journal of the Optical Society of America A, 1996, 13(5): 1106-1113.
[20] Gioux S, Mazhar A, Cuccia D J. Spatial frequency domain imaging in 2019: principles, applications, and perspectives[J]. Journal of Biomedical Optics, 2019, 24(7): 071613.
[21] Cuccia D J, Bevilacqua F P, Durkin A J, et al. Quantitation and mapping of tissue optical properties using modulated imaging[J]. Journal of Biomedical Optics, 2009, 14(2): 024012.
[22] CucciaD J, BevilacquaF, DurkinA J, et al. Depth-sectioned imaging and quantitative analysis in turbid media using spatially modulated illumination[C]∥ Biomedical Topical Meeting, April 14-17, 2004, Miami Beach, Florida. Washington, D.C.: Optica Publishing Group, 2004: FF5.
Article Outline
石志国, 张洋, 王全福, 李忠胜, 王霞, 董美丽, 倪敬书, 黄尧, 张盛昭, 王贻坤, 张元志. 偏振空间频域成像系统及仿体验证[J]. 中国激光, 2023, 50(9): 0907104. Zhiguo Shi, Yang Zhang, Quanfu Wang, Zhongsheng Li, Xia Wang, Meili Dong, Jingshu Ni, Yao Huang, Shengzhao Zhang, Yikun Wang, Yuanzhi Zhang. Polarization Spatial Frequency Domain Imaging System and Phantom Verification[J]. Chinese Journal of Lasers, 2023, 50(9): 0907104.