激光对魔芋葡甘聚糖降解的初步探究  下载: 799次
下载: 799次
1 引言
魔芋葡甘聚糖(KGM)因具有独特的凝胶性[1]、成膜性[2]、生物相容性[3]而被广泛应用于食品、化妆品、制药和保健品等领域[4-5],但天然KGM的分子质量大、黏度高[6],这在很大程度上限制了它的应用。因此,如何有效降解KGM已成为国内外研究的热点。
目前,降解KGM的方法主要有酸水解[7]、酶水解[8]、物理降解[9]和辐射降解[10]。李涛等[7]采用盐酸和过氧化氢对KGM进行降解,虽然该方法可在一定程度上降解KGM,但因盐酸存在易挥发、水解耗时长、会对环境造成一定程度的污染而无法被广泛应用;Jian等[8]采用甘露聚糖酶和γ射线对KGM进行降解,酶解温度为50 ℃,酶解时间为24 h,虽然通过该法能够获得分子质量小于1000 u的KGM寡糖,但存在着酶易失活、操作费时、程序繁琐等弊端;Li等[9]利用50 W的超声波在一定程度上实现了KGM的降解,降解时间为10~20 min,但是此法的收率较低,生产成本很高;Jin等[10]利用γ射线和乙醇对KGM进行降解,但乙醇在辐射过程中易挥发,导致其无法发挥应有的降解作用。
运用激光对大分子物质进行降解具有降解效率高、成本低、操作简单等优点[11]。例如,利用脉冲激光对2,4,5-三氯苯酚进行光催化降解,能够解决光子利用率低、反应器设计复杂、光催化剂的回收和固定化技术及光催化剂的污染与活化等许多降解问题;利用脉冲激光对废水中的苯酚进行降解能够大大提高降解速率,但将激光技术用于多糖降解的研究目前尚未见报道。此外,Pan等[12]曾采用γ射线和过氧化氢协同降解KGM,证明过氧化氢的存在会明显增强辐射降解的效果,且大量降解多糖的研究一致证明协同降解[13-15]比单一的物理、化学和生物降解方法更加高效。因此,本研究采用激光和过氧化氢协同降解KGM。
2 实验
2.1 激光操作参数
本研究采用的激光器为二氧化碳激光器[16-17],该激光器的效率高,可发射10.6 μm的可见红色激光,是一种比较理想的激光器。在其他条件相同的前提下,设定激光功率变化范围为7.5~15 W ,降解后的KGM的静态黏度见
表 1. 不同功率激光处理后KGM的黏度
Table 1. Viscosity of KGM after treatment with different laser powers
|
表 2. 激光器技术参数
Table 2. Technical parameters of laser
|
2.2 激光降解KGM
称取3.00 g KGM加入到300 mL蒸馏水中,以500 r/min的转速搅拌7 h,得到质量浓度为0.01 g/mL的KGM溶液;将其平均分为2组,A组样品平均分装在7个烧瓶中,再用功率为10 W的激光对7个样品分别进行0,1,2,3,4,5,6 min的激光处理,并标记为0号、1号、2号、3号、4号、5号、6号样品;在B组样品中加入体积分数为1.67%的过氧化氢,进行同样的激光处理,得到的样品分别记为0+号、1+号、2+号、3+号、4+号、5+号、6+号样品,示意图如
2.3 初步确定激光降解KGM较优条件的实验
2.3.1 黏度的测定
在常温下,使用NDJ-55型数字式粘度计分别测定A组、B组样品的黏度。
2.3.2 流变性能的测定
先将A组、B组样品在5000 r/min的转速下离心10 min,然后利用MCR301Rheoplus型流变仪进行剪切应力指标的测定,测试温度为25 ℃,剪切速率的范围为0.1 ~ 150 s-1。
2.4 KGM降解产物的表征
2.4.1 模量的测定
在常温下,利用MCR301Rheoplus型流变仪测定0号、0+号、2号、2+号样品的储能模量(
2.4.2 DSC的测定
将0号、0+号、2号、2+号样品进行24 h冷冻干燥后,利用200 F3型差示量热扫描仪进行差示扫描量热法(DSC)分析,温度范围为25 ~ 600 ℃,升温速率为15 ℃ · min-1。
2.4.3 红外光谱的测定
将0号、0+号、2号、2+号样品进行24 h冷冻干燥后,利用Cary 670-FTIR+610-FTIR光谱仪进行红外光谱的测定,测定波数范围为4000~400 cm-1,平行测量3次。
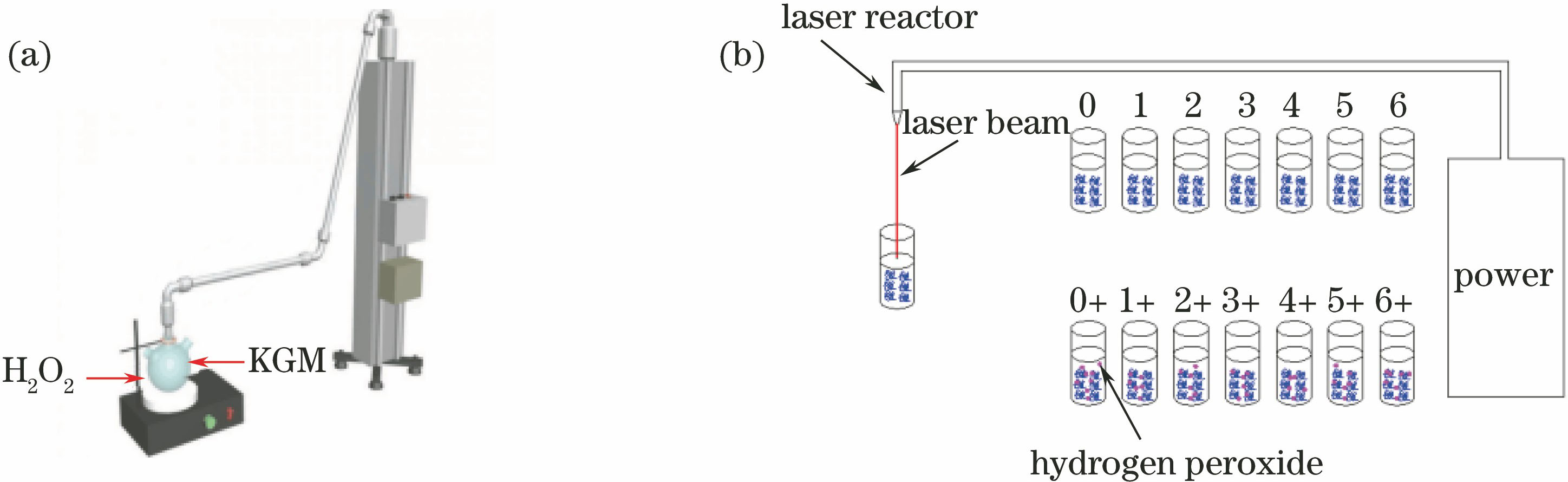
图 1. 激光处理示意图。(a)设备操作简图;(b)样品处理图
Fig. 1. Schematics of laser processing. (a) Diagram of equipment operating; (b) diagram of sample processing
3 实验结果
3.1 激光降解KGM较优条件的初步确定
3.1.1 黏度分析
激光处理时间对A组样品黏度的影响如

图 2. 激光处理时间对A组样品黏度的影响
Fig. 2. Effect of laser treatment time on viscosity of group A samples
由
激光处理时间对B组样品黏度的影响如

图 3. 激光处理时间对B组样品黏度的影响
Fig. 3. Effect of laser treatment time on viscosity of group B samples
3.1.2 流变性能分析
对激光功率为10 W,激光处理时间分别为0,1,2,3,4,5,6 min的两组样品分别进行静态剪切分析,剪切速率的变化范围为0.1~150 s-1,结果如
根据

图 4. 激光处理后KGM样品的稳定剪切黏度。(a) A组样品;(b) B组样品
Fig. 4. Stable shear viscosity of KGM samples after laser treatment. (a) Group A samples; (b) group B samples
3.2 KGM的模量
基于以上对KGM黏度和流变性能的分析,选取0号、0+号、2号、2+号样品进行模量分析,结果如
由
3.3 DSC分析
选取0号、0+号、2号、2+号样品进行DSC分析,结果如
DSC曲线可用来表征KGM在激光降解后的热稳定性。由
3.4 红外光谱分析
选取0号、0+号、2号、2+号样品进行红外光谱分析,结果如
由

图 7. 最佳降解条件下KGM的红外光谱分析
Fig. 7. FT-IR analysis of KGM under optimum degradation conditions
4 分析与讨论
激光照射后, KMG分子由原来的长链变成短链,在宏观上表现为KGM溶液的黏度降低,在微观上表现为

图 8. 激光降解机理图。(a)分子链断裂;(b) β-1,4糖苷键断裂
Fig. 8. Diagrams of laser degradation mechanism. (a) Molecular chain cleavage; (b) β-1,4 glycosidic bond cleavage
激光发射出的光子会促使H2O分解产生·OH,并且过氧化氢的加入会进一步增加其含量,从而增强激光的降解效果,具体反应如下[18-19]:
在激光辐射过程中,
通过如上的化学反应,在激光和过氧化氢同时存在的情况下,KGM溶液中的·OH浓度上升,而·OH是一种超氧化剂,极易夺取KGM分子链中与碳相连接的H原子,因此,最终会直接导致KGM分子链中的
5 结论
在激光功率为10 W,且有过氧化氢存在的条件下,激光和过氧化氢的共同作用可以促进
[5] Behera S S, Ray R C. Konjac glucomannan, a promising polysaccharide of Amorphophallus konjac, K. Koch in health care[J]. International Journal of Biological Macromolecules, 2016, 92: 942-956.
[6] Chua M, Baldwin T C, Hocking T J, et al. Traditional uses and potential health benefits of Amorphophallus konjac K. Koch ex N.E.Br[J]. Journal of Ethnopharmacology, 2010, 128(2): 268-278.
[7] 李涛, 马美湖, 邬应龙. 氧化-酸解法制备魔芋葡甘露低聚糖的初步研究[J]. 食品与发酵科技, 2009, 45(1): 35-39.
Li T, Ma M H, Wu Y L. Preliminary studies on degradation of konjac glucomannan with acid and H2O2[J]. Food & Fermentation Technology, 2009, 45(1): 35-39.
[11] 王狮凌, 房丰洲. 大功率激光器及其发展[J]. 激光与光电子学进展, 2017, 54(9): 090005.
[16] 李辉, 冯继东, 谭荣清, 等. 矩形波导CO2激光器谐振腔耦合效率研究[J]. 中国激光, 2017, 44(7): 0701003.
[17] 王振, 彭浩, 王炜, 等. 3 kW射频板条CO2激光器多电极放电均匀性与阻抗匹配性[J]. 光学学报, 2017, 37(3): 0314002.
Article Outline
林婉媚, 倪永升, 李源钊, 庞杰, 吴春华. 激光对魔芋葡甘聚糖降解的初步探究[J]. 激光与光电子学进展, 2018, 55(5): 051407. Wanmei Lin, Yongsheng Ni, Yuanzhao Li, Jie Pang, Chunhua Wu. Preliminary Study on Degradation of Konjac Glucomannan by Laser[J]. Laser & Optoelectronics Progress, 2018, 55(5): 051407.









