草甘膦溶液挥发物的表面增强拉曼光谱分析  下载: 1023次
下载: 1023次
1 引言
草甘膦(glyphosate),化学名为N-(膦酰甲基)甘氨酸,在现代生活中是一种比较常见的除草剂。将草甘膦喷洒在影响农作物生长的杂草中可有效抑制杂草的生长,使杂草枯死,达到除草的目的[1]。它被广泛应用于菜园、果园、农田、森林以及交通道路旁边等地的除草。目前,草甘膦已在世界范围内成为农药中应用范围最广、用量最大、年销售量最高的除草剂[2],但草甘膦的广泛使用使得土壤中、地表或地下水中形成草甘膦累积,造成严重的环境污染[3-5]。人和牲畜长期饮用有草甘膦残留的水或者吃有草甘膦残留的食物,药剂会在人和牲畜体内积累,积累达到一定程度就会对人和牲畜造成伤害。因此农药草甘膦残留量的检测对保证人们的身体健康具有十分重要的意义。
表面增强拉曼光谱(SERS)技术是一种使用粗糙金属表面的拉曼散射增强效应来对农药进行快速检测的光谱技术,具有高灵敏度、高分辨率、水干扰小、可猝灭荧光、稳定性好、可进行现场检测等优点,在农药快速检测领域具有广阔的应用前景[6-12]。已有一些文献报道了研究人员对草甘膦及其水溶液的SERS的相关研究[13-15],这些文献主要针对草甘膦纯品进行SERS的检测和研究。草甘膦是一种有机酸,常温下难溶于水(25 ℃时溶解度为1.2%),因此草甘膦需与碱性物质(如钾盐、胺盐、异丙铵盐等)反应生成盐以增加溶解度。同时由于草甘膦的展布性和润湿性较差,有效沉积少,单独使用除草效果并不理想。市场上销售的草甘膦农药都添加了各种助剂来增加其生物效能,而助剂的毒性远大于草甘膦纯品本身[16],因此对市售的草甘膦农药进行SERS研究更具有实际应用价值。同时许多农药都具有很大的挥发性,用SERS技术对农药在空气中的挥发物的检测鲜有相关的报道。本文用市售的农药草甘膦作为实验样品,以内壁吸附银纳米粒子的毛细玻璃管作为表面增强拉曼基底,对农药草甘膦在空气中的挥发物进行SERS研究,探索一种利用农药挥发物来检测农药残留量的新方法。
2 实验部分
2.1 仪器与试剂
实验所用仪器及试剂包括:激光共焦显微拉曼光谱仪(DXR,赛默飞世尔科技公司,美国),激发波长为780 nm;台式离心机(TGL-13G,上海安亭科学仪器厂,中国);毛细玻璃管(直径为1 mm,华西医科大学仪器厂,中国);硝酸银(浓度为99.8%);去离子水(电阻率为18.25 MΩ);草甘膦铵盐(重庆双丰化工有限公司,浓度为30%)。
2.2 银胶及毛细玻璃管表面增强拉曼基底的制备
银胶及毛细玻璃管表面增强拉曼基底的制备参照文献[
17-18]。银胶采用恒温法制备,配制浓度为10-3 mol/L的 AgNO3水溶液250 mL,配制浓度为1%的柠檬酸三钠水溶液7.5 mL,将二者充分混合后放入80 ℃的恒温水浴中,静置180 min,溶液变为灰绿色,这样就制成了实验所用的纳米银胶粒子。对银胶进行紫外-可见光吸收光谱表征,如
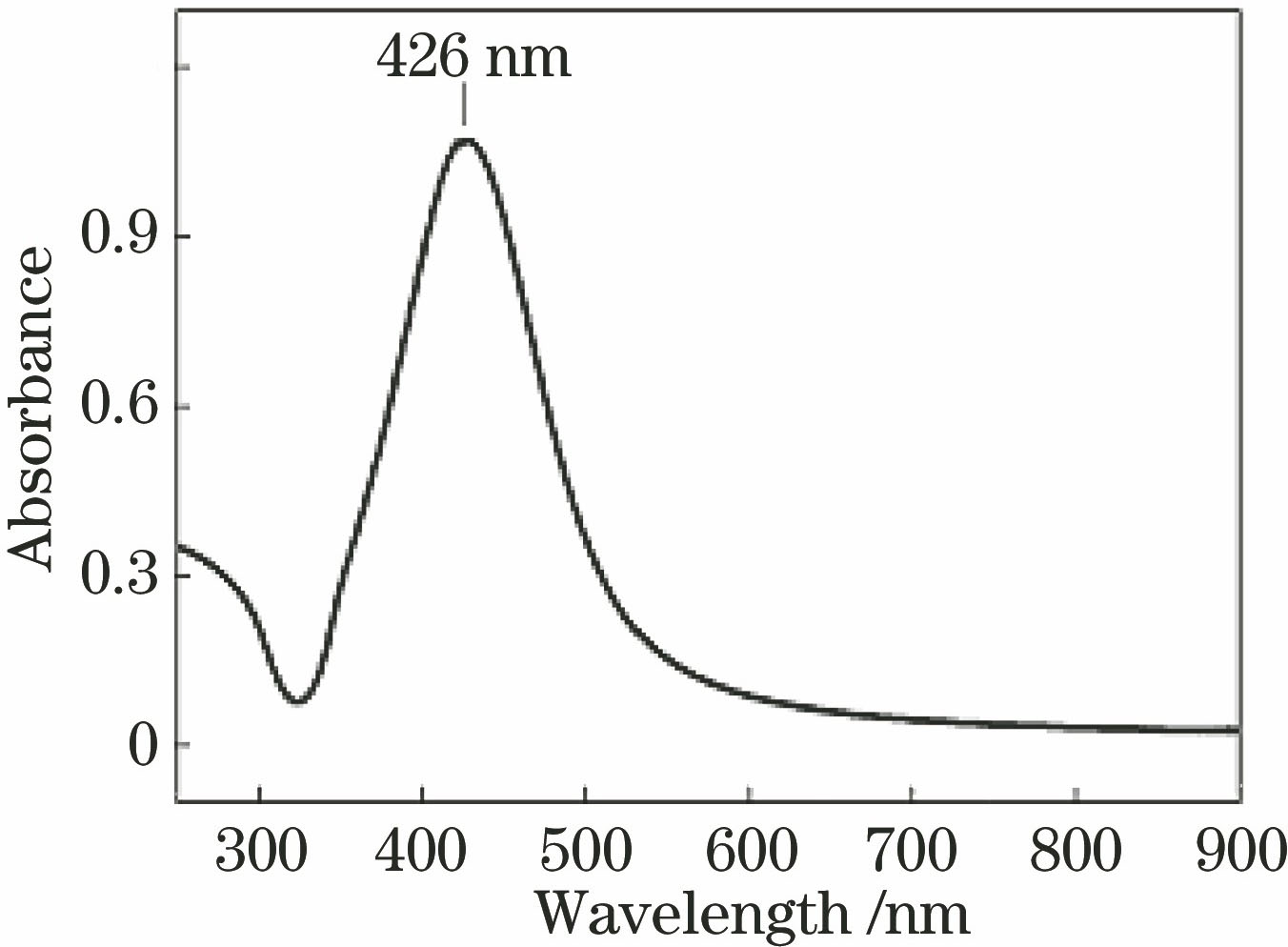
图 1. 银胶的紫外-可见光吸收光谱
Fig. 1. Ultraviolet-visible light absorption spectrum of prepared Ag colloid
把毛细玻璃管切成3 cm长的小段,放入干净的烧杯中用去离子水、乙醇和丙酮超声反复清洗3~4遍,每次清洗10 min。把清洗好的毛细玻璃管充分干燥后进行羟基化和硅烷化处理。把处理过的毛细玻璃管吸入浓缩过的银胶,静置约30 min,然后用大量的去离子水冲洗毛细玻璃管内壁,冲掉管内多余的银胶,最后用氮气把内壁吹干,这样就制备成了毛细玻璃管表面增强拉曼基底。毛细玻璃管表面增强拉曼基底内壁的扫描电子显微镜(SEM)照片如
备的毛细玻璃管表面增强拉曼基底是成功的。
2.3 草甘膦农药样品的制备
1) 草甘膦农药溶液样品的制备
将300 μL的草甘膦农药用去离子水稀释,依次制备成浓度为1.8×10-1,1.8×10-2,1.8×10-3,1.8×10-4,1.8×10-5,1.8×10-6 mol/L的草甘膦农药溶液备用。取制备好的银胶溶液滴在经过处理的载玻片上,待银胶溶液干燥后,用取样器将10 μL稀释好的不同浓度的农药草甘膦溶液分别滴在载玻片的银胶上面,并做好标记。
2) 草甘膦农药溶液挥发物样品制备
将300 μL的草甘膦农药用去离子水依次稀释成1.8×10-1,1.8×10-2,1.8×10-3,1.8×10-4,1.8×10-5,1.8×10-6 mol/L草甘膦农药溶液。把稀释好的草甘膦农药溶液放入密闭的小玻璃瓶中,然后将制备好的毛细玻璃管表面增强拉曼基底插入封闭的玻璃瓶口中,使草甘膦农药挥发物进入毛细玻璃管并吸附在毛细玻璃管内壁的银胶表面上。将含不同浓度的草甘膦挥发物样品的毛细玻璃管做好标记,用双面胶粘在载玻片上。
2.4 光谱采集
把制备好的草甘膦农药样品放入显微拉曼光谱仪中,测试SERS信号。物镜放大倍数为10倍,激光功率设定为2 mW,曝光时间为10 s,累积次数为10次。针对每个测试样品,分别采集5个SERS信号,取平均值来进行SERS研究。
3 结果与讨论
3.1 农药草甘膦样品的SERS分析
表 1. 农药草甘膦SERS特征峰及归属
Table 1. Characteristic peaks and affiliation of SERS of glyphosate pesticide
| ||||||||||||||||||||||||||||||||||||
3.2 不同浓度的草甘膦农药SERS分析
3.3 不同浓度的草甘膦农药挥发物SERS分析

图 5. 不同浓度草甘膦农药溶液挥发物的SERS
Fig. 5. SERS of volatiles of glyphosate with different concentrations
4 结论
采用恒温法制备银胶,毛细玻璃管内壁在经过化学方法处理后吸附了银纳米粒子制成表面增强拉曼基底。用所制备的基底对农药草甘膦溶液及其挥发物进行了SERS检测,得到了农药草甘膦溶液及其挥发物的SERS。通过对两种光谱的比较分析,发现草甘膦溶液挥发物SERS特征峰出现的位置与其溶液的SERS基本是一致的。但在某些位置,两者的特征峰存在很大的差别。用所制备的银胶作为基底测定了不同浓度草甘膦农药溶液的SERS,当草甘膦农药稀释到浓度为1.8×10-6 mol/L时仍然有明显的草甘膦农药的特征吸收峰。用所制备的毛细玻璃管银胶基底对不同浓度草甘膦农药溶液挥发物进行了SERS检测,当草甘膦农药溶液稀释到浓度为1.8×10-6 mol/L时,其挥发物仍然有明显的草甘膦农药特征吸收峰,说明本实验方法可以检测的草甘膦农药挥发物的浓度达到1.8×10-6 mol/L。其检测浓度已基本达到国家草甘膦农药残留最大检测标准,说明农药挥发物的SERS检测方法可作为检测草甘膦农药残留的一种快速有效的方法。同时此检测方法也可以为其他具有挥发性的农药残留的检测提供参考。本实验方法的基底制备没有特殊的要求,在一般的实验室中就能完成,便于在各个地方实施和应用。
[1] 何凯, 李国芳, 吴柱东, 等. 草甘膦分析方法的研究进展[J]. 理化检验(化学分册), 2011, 47(8): 991-995.
He K, Li G F, Wu Z D, et al. Recent progress of analytical methods for glyphosate[J]. Physical Testing and Chemical Analysis Part B(Chemical Analgsis), 2011, 47(8): 991-995.
[2] 苏少泉. 草甘膦述评[J]. 农药, 2005, 44(4): 145-149.
Su S Q. Glyphosate review[J]. Chinese Journal of Pesticides, 2005, 44(4): 145-149.
[3] Li F, Wang Y F, Yang Q Z, et al. Study on adsorption of glyphosate (N-phosphonomethyl glycine) pesticide on MgAl-layered double hydroxides in aqueous solution[J]. Journal of Hazardous Materials, 2005, 125(1/2/3): 89-95.
[4] Yue Y Y, Zhang Y H, Zhou L, et al. In vitro study on the binding of herbicide glyphosate to human serum albumin by optical spectroscopy and molecular modeling[J]. Journal of Photochemistry and Photobiology B: Biology, 2008, 90(1): 26-32.
[5] Kjaer J, Olsen P, Ullum M, et al. Leaching of glyphosate and amino-methylphosphonic acid from Danish agricultural field sites[J]. Journal of Environmental Quality, 2005, 34(2): 608-620.
[6] 张文强, 李容, 许文涛. 农药残留的表面增强拉曼光谱快速检测技术研究现状与展望[J]. 农业工程学报, 2017, 33(24): 269-276.
Zhang W Q, Li R, Xu W T. Research status and prospect of rapid detection technology of pesticide residues based on surface-enhanced Raman scattering[J]. Transactions of the CSAE, 2017, 33(24): 269-276.
[7] 吴燕, 彭芳, 吴斌, 等. 基于SERS技术的茶叶中乐果农药残留的快速检测[J]. 江苏农业科学, 2017, 45(14): 160-163.
Wu Y, Peng F, Wu B, et al. Rapid detection of dimethoate pesticide residues in tea based on SERS technology[J]. Jiangsu Agricultural Sciences, 2017, 45(14): 160-163.
[8] 黄林生, 王芳, 翁士状, 等. 表面增强拉曼光谱准确检测玉米中杀螟硫磷农药残留[J]. 光谱学与光谱分析, 2018, 38(9): 2782-2787.
[9] 李青龙, 王利华, 钟跃汉, 等. 表面增强拉曼光谱法快速检测香蕉中的噻菌灵[J]. 光谱学与光谱分析, 2018, 38(S1): 135-136.
Li Q L, Wang L H, Zhong Y H, et al. The fast detection of thiabendazole in fruit by SERS[J]. Spectroscopy and Spectral Analysis, 2018, 38(S1): 135-136.
[10] 卢树华, 王照明, 田方. 表面增强拉曼光谱技术在毒品检测中的应用[J]. 激光与光电子学进展, 2018, 55(3): 030004.
[11] 杨玥, 翁国军, 赵婧, 等. 纸质表面增强拉曼散射基底的制备及其应用进展[J]. 中国激光, 2018, 45(3): 0307011.
[12] 史晓凤, 张心敏, 严霞, 等. 基于三维表面增强拉曼基底的水中多环芳烃检测[J]. 光学学报, 2018, 38(7): 0724001.
[14] Sharma H S S, Carmichael E, McCall D. Fabrication of SERS substrate for the detection of rhodamine 6G, glyphosate, melamine and salicylic acid[J]. Vibrational Spectroscopy, 2016, 83: 159-169.
[15] Hilal T, Ismail H B. U ur T. Attomole detection of glyphosate by surface-enhanced Raman spectroscopy using gold nanorods[J]. Fabad Journal of Pharmaceutical Sciences, 2010, 35(4): 179-184.
[16] 杜勤惠, 孙道远. 草甘膦除草剂表面活性剂的毒性[J]. 中国工业医学杂志, 2018, 31(5): 368-371.
Du Q H, Sun D Y. Toxicities of surfactants in glyphosate-based herbicides[J]. Chinese Journal of Industrial Medicine, 2018, 31(5): 368-371.
[17] 张德清, 熊洋, 李伦, 等. 恒温法制备纳米银胶及其NIR-SERS活性研究[J]. 光散射学报, 2015, 27(3): 225-230.
[18] 杨永安, 张德清, 李伦, 等. 菜籽油中乐果农药残留表面增强拉曼光谱研究[J]. 激光生物学报, 2019, 28(2): 188-193.
Article Outline
杨永安, 张德清, 张川云, 司民真. 草甘膦溶液挥发物的表面增强拉曼光谱分析[J]. 激光与光电子学进展, 2020, 57(13): 133003. Yongan Yang, Deqing Zhang, Chuanyun Zhang, Minzhen Si. Surface Enhanced Raman Spectroscopy Analysis of Glyphosate Solution Volatiles[J]. Laser & Optoelectronics Progress, 2020, 57(13): 133003.









