基于Kanade-Lucas-Tomasi算法的人体体表呼吸运动追踪  下载: 1054次
下载: 1054次
1 引言
放射性疗法是治疗恶性肿瘤最有效的方法之一。据统计,欧洲恶性肿瘤的病人数量将在2025年突破450万[1],其中超过50%的病人可以通过放疗得到治愈[2-3]。如何提高放疗的精准度是放疗技术一直以来的研究热点,实现精准放疗需要在确保对肿瘤部位提供足够的照射剂量的同时确保照射束的准确性,既要对目标区域提供足够的辐照剂量又要尽可能地减少放疗照射束对周围正常组织及器官的伤害[4-5]。
当前国内临床的放疗手段多为在术前根据肿瘤的形态特征确定病人的放疗辐照区域并勾勒标记于病人体表、在手术中直接对指定区域进行照射治疗。但人体是一个非刚性结构,不同的组织器官存在非同步的运动状态,并且人体的心跳和呼吸运动也具有一定的运动复杂度,两者都不遵循严格的周期性和线性。这就会导致人体的组织器官在手术过程中会随着患者的心跳和呼吸产生难以预计的形变和位移[6-10]。实验发现,在人体呼吸运动过程中,肺部会在上下、左右、前后三个方向分别移动(2.4±1.3) mm、(2.4±1.4) mm 和(3.9±2.6) mm[11],HOISAK团队利用透视法得到病人在静息态下肺下叶肿瘤的上下运动幅度为14.3mm[12],这就可能导致治疗过程中的放疗射线会照射到治疗部位以外的正常组织和器官,引发器官组织炎症并诱发其他并发症,不利于病人的治疗和康复。呼吸运动还会导致肿瘤溢出目标范围,使得针对肿瘤区域的辐照剂量不足,影响治疗效果。在这种情况下,控制呼吸运动造成的误差以提高放疗的精准程度就成为了一个亟待解决的问题。
目前解决这个问题的方案主要有两种。一种是在放疗过程中对肿瘤进行实时监测和追踪,并根据肿瘤的实时位置对射线进行调整[13];该方案准确率高,但技术实现难度大,对硬件设备要求高,难以在短时间内实现该方案在医疗场所的普及。另一种方案是在手术过程中对病人的呼吸运动进行量化,同时获取病人的实时呼吸运动信息,以此来指导手术进行[14]。针对呼吸运动检测问题,当前国内外在临床上主要的技术方案有屏气或腹部压迫、呼吸门控、四维放射性疗法及实时追踪技术等。其中,通过主动或被动屏气技术控制患者的呼吸或压迫腹部以减少肿瘤及周围器官的运动的方法是直接且可行的,但这种方法需要患者自身肺部功能基本正常且接受了一定时间的呼吸训练,对急症或肺部损伤的病人并不适用,因此该方案的耐受性较差[15]。呼吸门控技术可以调整放射束的辐照时间与病人呼吸周期的特定时间相同步,以此来减少辐照期间肿瘤在窗口中的移动。但线性加速器的选择性打开延长了加速器的工作周期,使得治疗时长成倍增加[16]。三维立体放疗技术能够获取人体内部结构及器官的实时位置信息,为肿瘤定位、治疗方案的制定提供技术支持。但该技术的实施需要持续的透视图像采集,过长的辐照时间不但会对患者造成二次伤害,而且容易在纵方向上产生伪影。同时术前对患者的平稳呼吸培训也增加了技术实施难度。近几年也有一些新技术的出现,但这些技术也存在其他的缺点和问题[17]。综上所述,手术中对病人的呼吸运动进行直观而准确的定量分析,对临床上指导精准放疗具有现实意义,通过对患者呼吸运动的实时表征,可以灵活调整射线和治疗床的位置,确保射线和目标肿瘤一直处于稳定的相对位置上。
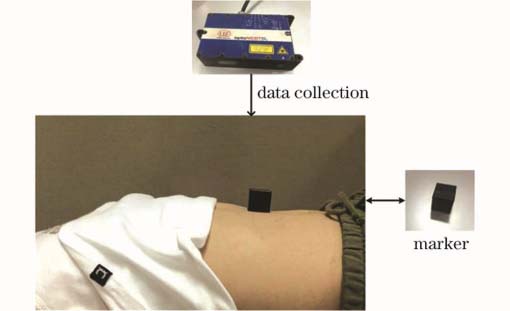
当前大多数的实时追踪算法仅在追踪刚体时有出色的表现,但人体表面属于非刚性结构且会随着呼吸运动产生不规则的波动及形变。为解决这个问题,实验中采用一个刚性体表标记物作为追踪目标进而实现对体表的实时追踪。实验结果表明,利用追踪体表标记物可以实现对人体体表呼吸运动的表征,并获取实时呼吸运动曲线以及位移和角度变化等参数。通过对比实验测试结果和实际位移值,验证了实验算法的可靠性。
2 实验
2.1 实验场景搭建
实验1采集了实验对象在5个自然呼吸周期下的图像信息,并通过激光位移传感器测得人体体表的实时位移变化量。将体表的实际位移与算法预测的感兴趣区域(ROI)的左下角点帧间像素差进行对比,验证了实验方案的可行性。实验场景如
为了准确地控制实验变量,实验2将实验对象替换为仿真体模,在中国科学院近代物理研究所深层肿瘤治疗实验室进行实验。实验场景图如
2.2 实验过程
为验证最佳追踪效果的拍摄角度,实验2通过调整摄像头的位置,分别从三个角度(即水平侧视、从顶部向下俯视、从底部向上仰视)对体模进行图像采集。其中,水平侧视采用与实验1相同的位置参数:摄像头与标记物保持水平,距离标记物50cm,激光位移传感器距离标记物上表面50cm;从顶部向下俯视采集时,将摄像头置于体模头部上方,并使其与标记物保持水平,且距离标记物50cm,激光位移传感器距离标记物上表面50cm;对于从底部向上采集的仰视视角,将摄像头置于体模脚部下方,使其与标记物保持水平,其距离标记物50cm,激光位移传感器距离标记物表面50cm。
在确定图像采集视角后,考虑到放疗过程中的患者可能会由于各种突发状况出现不同的呼吸表现,设定三组参数来模拟病人最常见的三种呼吸模式:正常呼吸(振幅15mm,频率20次/min),微弱呼吸(振幅10mm,频率10 次/min),急促呼吸(振幅8mm,频率23次/min)。同时将激光位移传感器安装在固定支架上,调整激光射线使光斑对准标记物上表面的中心点位置,图像采集视角都为水平侧视。最后将激光位移传感器反馈的位移量与标记物角点的帧间像素差进行比较,得到实验结论。该算法的应用及验证都是在MATLAB 6.0 (MathWorks Inc.)上实现的。
2.3 图像预处理
为了减少背景中其他运动物体对标记物追踪的干扰,采用帧间处理的方法来提升追踪效果,并将处理后的图像降采样到每帧图像大小为540pixel×960pixel(每像素大小为0.58mm×0.58mm)。对降采样后的图像进行两个阶段的预处理:边缘增强和边缘检测。考虑到传统的均值滤波器有模糊边缘的缺点,为了保留标记物完整的边缘信息,依次选用一个模板为15×15、噪声方差为155的Lee滤波器,一个模板为13×13的Kuwahara滤波器,以及一个方差为1的局部零均值高斯滤波器对图像进行去噪,再使用“5抽头系数”的方法计算图像的梯度幅度和方向,得到边缘增强结果。图像的边缘信息使用Canny边缘检测算子来检测得到。预处理流程图如
2.4 Kanade-Lucas-Tomasi算法
Kanade-Lucas-Tomasi(KLT)算法一种是基于特征点的目标追踪算法,是光流法的一种。它的提出主要基于三个假设条件:恒定的亮度、一致的空间以及微小的运动。以上三个假设是为了确保:1)目标不受亮度影响;2)可以在目标区域找到特征点;3)在同一窗口中所有特征点的位移大小都相等。该算法最先由Lucas和Kanade提出[18],他们将图像配准问题从传统的滑动窗口搜索方式转变为计算像素点偏移量的过程。后来,Shi和Tomasi[19]对KLT算法进行了进一步完善,给定图像
式中:
式中:
KLT算法依靠特征点匹配实现追踪,因此选取的特征点的质量直接影响到最后的追踪结果,而角点由于其丰富的形状信息,尤其适合作为特征点。将物体角点作为特征点的Harris角点检测算法具有良好的鲁棒性和定位能力,此外还能够很好地适应目标的旋转和缩放,因此本研究选取Harris算法作为角点检测算法。
2.5 感兴趣区域追踪
首先利用摄像头将采集到的图像上传到计算机,此时需要手动标记第一帧图像中标记物的4个角点以获取追踪的初始帧图像。ROI区域的宽度
将4个角点横坐标的最大值
式中:
3 实验结果
3.1 图像预处理结果

图 5. 预处理结果示意图。(a)原始图像;(b)降采样后的图像;(c)经过Lee滤波器后的图像;(d)经过Kuwahara滤波器后的图像;(e)经过高斯滤波器后的图像;(f)采用Canny算子进行图像边缘检测后的结果
Fig. 5. Results of pre-processing. (a) Original image; (b) down-sampled image; (c) image filtered by Lee filter; (d) image filtered by Kuwahara filter; (e) image denoised by Gaussian filter; (f) edge detection result with Canny operator
3.2 实验1结果
实验采集受试者25s的呼吸过程进行实验。实验1的结果如
式中:

图 6. 实验1追踪结果。(a)手动标定第一帧图像中标记物的4个角点;(b)算法根据手动标定的角点位置计算出的ROI; (c)KLT算法对第100帧图像的追踪结果
Fig. 6. Tracking results of experiment 1. (a) Mark four corner points of marker in first frame manually; (b) ROI calculated by algorithm according to marked coordinates of corner points; (c) tracking result of 100th frame with KLT algorithm
表 1. 实际位移与帧间像素差值的对比表
Table 1. Table of comparison of actual displacement and pixel difference between frames
|
实验中激光位移传感器的采集频率为624Hz,远大于算法追踪频率。为了使实验与算法处理图像的帧数相一致,将传感器采集的数据从18027降采样到398。另外,考虑到激光位移传感器与摄像头没有统一的触发开关,传感器的数据采集时长稍长于摄像头,因此仅保留了前370帧的数据用于绘制对比曲线,结果如

图 7. 体表实际位移与ROI角点纵坐标帧间像素差的对比曲线
Fig. 7. Curves of actual displacement of body surface and pixel difference between ordinate frames of ROI corner points
3.3 实验2结果
实验1已经验证可以通过一个体表标记物来表征体表的呼吸运动,而算法在图像中框选的就是算法预测的标记物的实时位置,以及ROI角点及中心点的实时位置坐标、旋转角度及帧间像素差等信息。为进一步验证算法表征呼吸运动的准确性,通过调整仿真体模的相关参数,模拟人体在三种不同呼吸状态下的运动信息(正常呼吸:振幅15mm,频率20次/min;微弱呼吸:振幅10mm,频率10次/min;急促呼吸:振幅8mm,频率23 次/min)进行追踪实验。

图 9. 三种呼吸状态下体模运动曲线及算法追踪曲线对比。(a)三种呼吸状态;(b)体模运动曲线;(c)算法追踪曲线
Fig. 9. Comparison of phantom motion curves and algorithm tracking curves under three breathing conditions. (a) Three breathing conditions; (b) phantom motion curves; (c) algorithm tracking curves
为进一步验证追踪的准确性,将算法预测的ROI中心点的帧间坐标像素差与标记物的实际位移进行对比。虽然人体的呼吸运动不遵循严格的周期性,但体表在呼吸运动过程中的上下起伏存在一定的规律,经观察发现,每40帧的图像间隔可以有效表述一个呼吸运动周期。
表 2. 标记物实际位移量与ROI中心点位置变化对比表
Table 2. Comparison of actual displacement and changes in position of central point of ROI
|
为更清晰地量化两组数据的误差,选取前800帧图像,将其分为20组,对数值进行归一化处理,依据

图 10. 标记物实际位移与特征点像素差对比曲线
Fig. 10. Actual displacement of marker and pixel difference between feature points
追踪算法常见的一个问题是追踪效果会随实验时长的增加而变差。而追踪效果的持续性和稳定性被认为是追踪任务的关键指标。为探讨本实验算法在完成呼吸追踪任务时的稳定性表现,在正常呼吸模式下重复实验3次,依次选取实验结果的第2帧、第100帧、第150帧、第200帧及第250帧图像,将选取图像的ROI特征点像素差与标记物的实际位移相比较,绘制如
4 结论
针对放疗场景下人体呼吸运动实时监测的问题,提出了一种基于KLT算法的通过追踪体表标记物表征体表呼吸运动的方法。经实验验证,该方法能在实时表征人体呼吸运动的同时,提供呼吸频率、呼吸幅值、呼吸状态变化等关键信息,为放疗手术提供数据参考。实验结果表明,算法追踪得到的呼吸运动曲线与实际呼吸运动曲线基本重合,归一化后实际误差小于0.03。
相比于其他技术难度大、实现复杂的呼吸监测方法,所提出的方法仅需要一个摄像头,通过图像处理算法即可有效采集人体呼吸运动的实时信息,这不仅降低了操作难度,更减少了传统磁共振成像呼吸监测方案对病人的辐照伤害,所提算法能够以更低的成本、更高的追踪精度实现患者的呼吸运动管理。
实验2确定了水平侧视为最佳图像采集视角,在其他两个视角下,ROI与目标的实际位置存在偏差的可能原因是:随着呼吸运动的进行,标记物的左下和右下两个角点被模型的主体部分遮挡,在角点检测中仅剩余两个角点被测得,而ROI的尺寸信息是基于第一帧图像计算得到的。因此在后续的ROI位置预测时,算法会按照已确定的ROI大小,基于检测到的两角点来绘制ROI,这就可能造成较大的追踪误差。虽然Harris角点检测是逐帧进行,当丢失的特征角点再次出现时算法就会自动校正,只要采样频率足够高,实际误差不会对真实场景的检测造成影响。但在某些视角下,丢失的角点可能在长时间内不会再次出现,算法就失去了自我校正的能力。事实上,在设计算法时,可以按照图像情况减少选择的特征点个数并绘制ROI,但这会降低ROI生成和追踪的准确率,本研究中不能以牺牲准确率为代价提升追踪的稳定性。因此,应通过选择最佳的拍摄角度来解决特征角点被遮挡的问题。
此外,在验证实验中,特征点的帧间像素差及标记物的实际位移皆为取自竖直方向上的量,其原因是算法得到的特征点纵坐标帧间平均差值为0.48pixel,而横坐标帧间平均差值为0.02pixel。因此呼吸运动在竖直方向上的运动范围更大,运动趋势也更加明显,进而能够更准确地表征呼吸运动。
实验算法的计算复杂度较高,如何在不降低追踪精度的前提下提高计算速度将是下一步工作的重点。
[1] Global CancerObservatory. Report of WHO Scientific Group[R]. Geneva: WHO, 2019: 3.
[3] Atun R, Jaffray D A, Barton M B, et al. Expanding global access to radiotherapy[J]. The Lancet Oncology, 2015, 16(10): 1153-1186.
[6] Scholz M, Kellerer A M, Kraft-Weyrather W, et al. Computation of cell survival in heavy ion beams for therapy[J]. Radiation and Environmental Biophysics, 1997, 36(1): 59-66.
[7] Krämer M, Jäkel O, Haberer T, et al. Treatment planning for scanned ion beams[J]. Radiotherapy and Oncology, 2004, 73: S80-S85.
[8] Phillips M H, Pedroni E, Blattmann H, et al. Effects of respiratory motion on dose uniformity with a charged particle scanning method[J]. Physics in Medicine and Biology, 1992, 37(1): 223-234.
[10] Berson A M, Emery R, Rodriguez L, et al. Clinical experience using respiratory gated radiation therapy: Comparison of free-breathing and breath-hold techniques[J]. International Journal of Radiation Oncology * Biology * Physics, 2004, 60(2): 419-426.
[11] Ekberg L, Holmberg O, Wittgren L, et al. What margins should be added to the clinical target volume in radiotherapy treatment planning for lung cancer?[J]. Radiotherapy and Oncology: Journal of the European Society for Therapeutic Radiology and Oncology, 1998, 48(1): 71-77.
[12] Hoisak J D P, Sixel K E, Tirona R, et al. Correlation of lung tumor motion with external surrogate indicators of respiration[J]. International Journal of Radiation Oncology * Biology * Physics, 2004, 60(4): 1298-1306.
[13] Urschel HC, Jr, Kresl J J, Luketich J D, et al. Treating tumors that move with respiration[M]. Heidelberg: Springer, 2007.
[14] Eccles C, Brock K K, Bissonnette J P, et al. Reproducibility of liver position using active breathing coordinator for liver cancer radiotherapy[J]. International Journal of Radiation Oncology * Biology * Physics, 2006, 64(3): 751-759.
[15] WangJ, BorsdorfA, HeiglB, et al.Gradient-based differential approach for 3-D motion compensation in interventional 2-D/3-D image fusion[C]//2014 2nd International Conference on 3D Vision, December 8-11, 2014, Tokyo, Japan.New York: IEEE Press, 2014: 293- 300.
[17] 刘航, 汪西莉. 基于注意力机制的遥感图像分割模型[J]. 激光与光电子学进展, 2020, 57(8): 081002.
[18] Lucas BD, KanadeT. An iterative image registration technique with an application to stereo vision[C]// Proceedings of the 1981 DARPA Image Understanding Workshop,San Francisco: Morgan Kaufmann Publishers Inc., 1981: 121- 130.
[19] ShiJ, TomasC. Good features to track[C]//1994 Proceedings of IEEE Conference on Computer Vision and Pattern Recognition, June 21-23, 1994, Seattle, WA, USA.New York: IEEE Press, 1994: 593- 600.
Article Outline
刘昕宇, 闫铮, 段放, 戴中颖. 基于Kanade-Lucas-Tomasi算法的人体体表呼吸运动追踪[J]. 激光与光电子学进展, 2020, 57(22): 221001. Xinyu Liu, Zheng Yan, Fang Duan, Zhongying Dai. Tracking of Human Respiratory Motion Based on Kanade-Lucas-Tomasi Algorithm[J]. Laser & Optoelectronics Progress, 2020, 57(22): 221001.