甲硝唑的太赫兹特征吸收光谱分析  下载: 1012次
下载: 1012次
1 引言
甲硝唑(2-甲基-5-硝基咪唑-1-乙醇)主要用于治疗肠道和肠外阿米巴病(如阿米巴肝脓肿、胸膜阿米巴病等),还用于治疗阴道滴虫病、小袋虫病和皮肤利什曼病,以及麦地那龙线虫感染和厌氧菌感染[1-2]。由于药物的残留、交叉抗药性、品质控制直接关系到人们的生命安全,因此,寻求一种对药物残留进行快速、无损检测的手段非常重要。目前,医学上常用的检测方法主要有理化检测方法和微生物检测法。气相色谱法、分光光度法等属于理化检测方法,这些方法的检测程序比较复杂,检测费用较高;氯化三苯基四氮唑法属于微生物检测法,该方法的测定时间较长,且测量结果误差较大[3-4]。此外,常用的检测方法还有紫外鉴别法和红外吸收法,但人们对抗生素药品的结构关系和稳定性等缺乏全面的认识[5-6]。化学生物分子的太赫兹光谱包含着丰富的光谱和结构信息,具有高度的专属性和特异性[7-8],许多分子的振动和转动跃迁、分子间的弱相互作用(如氢键、范德瓦耳斯力等)以及晶格的低频振动等都位于太赫兹波段。因此,利用太赫兹时域光谱技术对甲硝唑进行研究具有重要意义。
太赫兹波在电磁波谱中介于微波与红外波之间,它的振荡频率在1012 Hz附近。太赫兹波的频率范围在0.1~10 THz之间[9]。太赫兹波相较于其他电磁波具有很多特殊性质,如安全性、透视性、瞬态性、相干性以及指纹特性。随着太赫兹技术的发展,其应用前景也越来越广阔,易被广泛应用于航空航天、安全检查、质量控制、医疗诊断以及生物和化学制剂的检测过程中[10-13]。目前,已有许多研究人员就太赫兹技术在药品检测领域的应用进行了大量研究,如:2011年,Redo-Sanchez等[14]研究了家畜常用的11种抗生素的光谱特性,并采用太赫兹技术检测了食品中的抗生素残留;2015年,Xie等[15]研究了卡那霉素的太赫兹光谱,并在超表面上检测出了微量硫酸卡那霉素;2017年,黄玉等[16]对拉西地平的太赫兹光谱进行了实验研究;同年,Qin等[17]使用衰减全反射太赫兹时域光谱法对盐酸四环素溶液进行了研究;2018年,Long等[18]利用太赫兹光谱法分析了饲料基质中氟喹诺酮类抗生素的残留。
本研究分别利用太赫兹时域光谱技术和高效液相色谱法这两种检测手段对硝基咪唑类抗生素中的甲硝唑分析纯与口服甲硝唑进行检测,并以密度泛函理论为理论基础,计算甲硝唑在太赫兹波段的特征吸收理论峰值,以期为抗生素的快速无损检测和质量评价提供依据。
2 实验方法与样品制备
2.1 实验方法
高效液相色谱实验装置采用美国塞默飞世尔公司的双三元、二维液相色谱仪系统UltiMate 3000 DGLC,该系统的进样量为10 μL,检测波长为280 nm。太赫兹光谱检测实验装置采用美国Zomega公司的Z-3型典型太赫兹时域光谱系统,该系统以光电导天线作为太赫兹辐射源,ZnTe作为探测晶体。飞秒激光器产生的光脉冲的中心波长和重复频率分别为800 nm和80 MHz,飞秒激光经分束镜后被分为泵浦光和探测光两束光。实验系统获得的太赫兹信号的频谱范围为0.2~2.0 THz。为减小空气中的水汽对测试结果的影响,在室温及干燥的氮气(相对湿度<1%)环境下进行测试。
将采集的样品的时域信号和参考时域信号进行傅里叶变换(FFT),转换为频域信号Esam(ω)和Eref(ω),得到振幅比和相位差。折射率公式为
吸收系数的近似计算公式为
式中:φ(ω)为相位差,φ(ω)=φsam-φref;c为真空中的光速;ω为角频率;d为样品厚度;ρ(ω)为振幅比,ρ(ω)=Asam/Aref,A为振幅。
测试时,为了减小实验误差,每一个样品取3次检测结果的平均值后再进行数据处理。吸收光谱采用Savitzky-Golay滤波进行平滑处理,Point of window设置为30,Polynomial order设置为2。
2.2 样品制备
实验使用的甲硝唑分析纯购于生工生物工程(上海)股份有限公司(批号:E807BA0049),纯度为98.1%;口服甲硝唑购于华中药业股份有限公司。实验样品均为多晶体粉末,使用前均未经过进一步纯化处理。
高效液相色谱法被广泛用于药品质量的评价。按照药典及相关文献配制液相色谱测试样品溶液和流动相。首先,量取甲醇分析纯200 mL,加超纯水稀释至1 L,配制流动相;然后,用抽滤装置将流动相过滤;接着,精密称取甲硝唑分析纯和口服甲硝唑粉末各10.0 mg,并将它们分别放入容量为250 mL的烧杯中,用流动相进行超声溶解;然后,将过滤后的样品溶液倒入容量为25 mL的容量瓶中,用流动相定容,摇匀后再次进行超声溶解,直至溶液澄清为止;最后,用一次性吸管取续滤液约1 mL作为测试样品溶液,将剩余的测试样品放入冰箱(温度为4 ℃)中保存。
聚乙烯粉末(PE)在太赫兹波段范围内没有特征吸收,因此在制样时向两种甲硝唑样品中添加市销PE标准品,以减小样品过量带来的强吸收的影响;同时,为了减小样品散射的影响,对混合样品粉末进行了充分的研磨,并使用200目细胞筛进行筛选,直至样品表面无明显的反射光。最终的甲硝唑分析纯和口服甲硝唑溶液均按4个浓度梯度(质量分数分别为20%、30%、40%、50%)配制。制样时采用压片的方式将混合粉末压制成薄片,压力设置为19600 N,保压时间为2 min,将样品压制成厚度约为1.5 mm、直径为13 mm、质量为200 mg的均匀片状样品。薄片样品的结构均匀,两端面平行。
3 实验结果与分析
3.1 液相色谱测试结果
根据《中国药典》中配制液相色谱测试样品的方法,流动相采用甲醇水溶液(溶液中甲醇的质量分数为20%),设定检测波长为315 nm,测试结果如
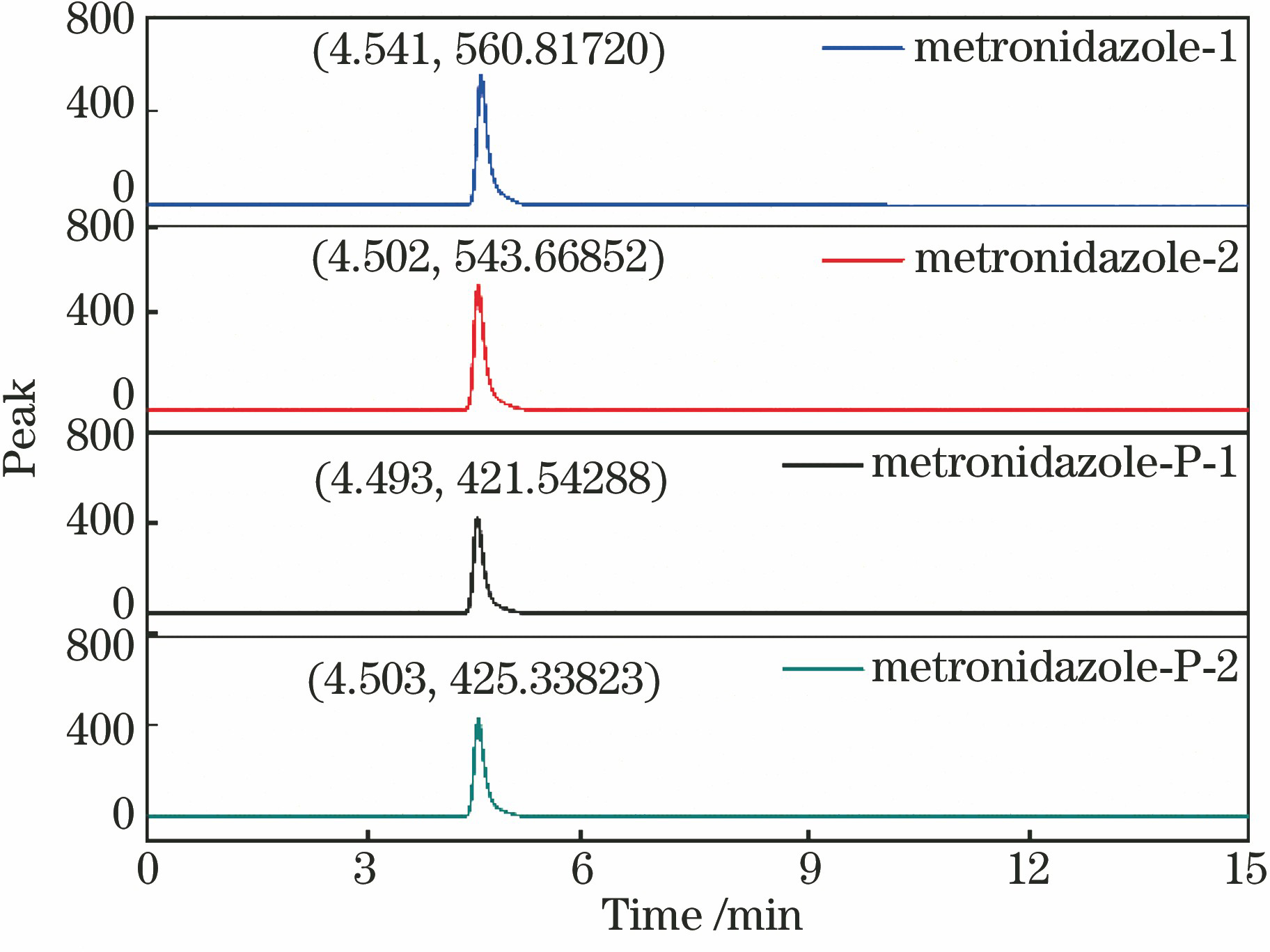
图 1. 甲硝唑分析纯和口服甲硝唑的液相色谱图
Fig. 1. Liquid chromatograms of metronidazole analytical pure and oral metronidazole

图 2. 甲硝唑分析纯的时域光谱和吸收光谱。(a)时域光谱;(b)吸收光谱
Fig. 2. Time-domain and absorption spectra of metronidazole analytical pure. (a) Time-domain spectrum; (b) absorption spectrum
3.2 太赫兹时域光谱测试结果
本文对不同浓度的甲硝唑分析纯进行了测试,测试结果如
此外,本文还对口服甲硝唑进行了太赫兹光谱检测,其中口服甲硝唑的配样浓度为20%~50%(质量分数),检测结果如

图 3. 口服甲硝唑的时域光谱和吸收光谱。(a)时域光谱;(b)吸收光谱
Fig. 3. Time-domain and absorption spectra of oral metronidazole. (a) Time-domain spectrum; (b) absorption spectrum
3.3 理论计算结果与分析
本研究采用Materials Studio软件中的Dmol3模块计算甲硝唑的分子振动频率,解析甲硝唑的特征吸收峰。晶体模拟计算分为建模、结构优化和频率计算三部分。建模时使用的甲硝唑分子结构来源于剑桥晶体结构数据库,甲硝唑的晶格参数如下:空间群为P21/c(14),a=0.69446(4) nm,b=0.86853(7) nm,c=1.23900(10) nm,α=90°,β=94.4380(10)°,γ=90°。甲硝唑的分子结构图如
在计算甲硝唑晶体的振动频率时选择多种交换-关联函数广义梯度近似中的PW91,基组均设置为DND,收敛精度为“Fine”。甲硝唑理论计算的低频部分如
表 1. 甲硝唑振动频率的计算结果
Table 1. Calculated vibration frequency of metronidazole
|
通过对比发现,函数PW91计算结果中的1.379 THz、1.704 THz与实验结果最为相近,但仍有一些偏差。出现偏差的原因可能如下:1)模拟计算时使用Dmol3软件进行密度泛函计算,振动频率均为分子模型在0 K温度下获得的,而实验环境为室温,与模拟计算的环境变量有所不同;2)实验获得的甲硝唑的太赫兹吸收光谱由分子内的振动、分子间的相互作用(如氢键、范德瓦耳斯力)、大分子的骨架振动以及晶格振动和声子模式等组成,而本文的理论建模主要采用晶体结构,并未考虑晶格低频振动和声子模式对样品特征吸收峰的影响;3)不同的函数计算结果也有偏差。选择不同的函数和采用不同的估算方式都会得到不同的计算结果,计算时不能只采用某一种单一的计算函数,因为一种函数的模拟结果并不能准确地表征实验现象。

图 5. 甲硝唑在1.36 THz处的分子振动模式
Fig. 5. Molecular vibrational mode of metronidazole at 1.36 THz
使用Materials Studio软件中的可视化模块对甲硝唑晶体特征吸收峰的形成机制进行指认。甲硝唑在1.36 THz和1.67 THz处的分子振动模式如

图 6. 甲硝唑在1.67 THz处的分子振动模式
Fig. 6. Molecular vibrational mode of metronidazole at 1.67 THz
4 结论
通过实验检测了不同浓度甲硝唑分析纯和口服甲硝唑溶液的太赫兹光谱,获得了甲硝唑分析纯和口服甲硝唑在0.2~2.0 THz范围内的吸收特征峰。实验结果表明,甲硝唑样品具有显著的太赫兹光学吸收特性。使用高效液相色谱法测试了两种甲硝唑样品,结果显示,口服甲硝唑的主成分与甲硝唑分析纯的主成分一致。
高效液相色谱法和太赫兹时域光谱法的测试结果具有较好的一致性,进一步证实了太赫兹光谱技术快速识别甲硝唑等抗生素残留的可行性。模拟计算了甲硝唑在太赫兹波段的吸收光谱的理论峰值,并对特征峰吸收峰的振动模式进行了指认。太赫兹时域光谱技术检测甲硝唑的流程更为快速简便,太赫兹这一有效的表征手段可为进一步了解抗生素分子结构变化提供有力的技术支撑,对临床医学上相关的快速检测具有重要意义。
[2] Doron SI, Beaulac KR, DhandA, et al.Mechanisms of resistance in metronidazole[M] ∥Antimicrobial Drug Resistance. Cham: Springer International Publishing, 2017: 281- 287.
[3] Bhatia S C, Shanbhag V D. Electron-capture gas chromatographic assays of 5-nitroimidazole class of antimicrobials in blood[J]. Journal of Chromatography B, 1984, 305: 325-334.
[4] Becke A D. Density-functional thermochemistry. III. The role of exact exchange[J]. The Journal of Chemical Physics, 1993, 98(7): 5648-5652.
[5] 张振伟, 左剑, 张存林. 甲硝唑、替硝唑和奥硝唑药品的远红外与太赫兹吸收光谱研究[J]. 光谱学与光谱分析, 2012, 32(4): 906-909.
[6] Chinese PharmacopoeiaCommission. Pharmacopoeia of the People's Republic of China[M]. Beijing: China Medical Science Press, 2015.
[8] Melinger J S, Harsha S S, Laman N, et al. Temperature dependent characterization of terahertz vibrations of explosives and related threat materials[J]. Optics Express, 2010, 18(26): 27238-27250.
[9] 张希成, 许景周. 太赫兹科学技术和应用[M]. 北京: 北京大学出版社, 2007.
Zhang XC, Xu JZ. Terahertz science, technology and application[M]. Beijing: Peking University Press, 2007.
[10] Strachan C J, Rades T, Newnham D A, et al. Using terahertz pulsed spectroscopy to study crystallinity of pharmaceutical materials[J]. Chemical Physics Letters, 2004, 390(1/2/3): 20-24.
[11] Walther M, Plochocka P, Fischer B, et al. Collective vibrational modes in biological molecules investigated by terahertz time-domain spectroscopy[J]. Biopolymers, 2002, 67(4/5): 310-313.
[12] Ferguson B, Zhang X C. Materials for terahertz science and technology[J]. Nature Materials, 2002, 1(1): 26-33.
[13] Duvillaret L, Garet F, Coutaz J L. Highly precise determination of optical constants and sample thickness in terahertz time-domain spectroscopy[J]. Applied Optics, 1999, 38(2): 409-415.
[14] Redo-Sanchez A, Salvatella G, Galceran R, et al. Assessment of terahertz spectroscopy to detect antibiotic residues in food and feed matrices[J]. The Analyst, 2011, 136(8): 1733-1728.
[15] Xie L, Gao W, Shu J, et al. Extraordinary sensitivity enhancement by metasurfaces in terahertz detection of antibiotics[J]. Scientific Reports, 2015, 5: 8671.
[16] 黄玉, 孙萍, 张正, 等. 拉西地平的太赫兹光谱实验研究[J]. 光谱学与光谱分析, 2017, 37(8): 2356-2359.
[17] Qin J Y, Xie L J, Ying Y B. Rapid analysis of tetracycline hydrochloride solution by attenuated total reflection terahertz time-domain spectroscopy[J]. Food Chemistry, 2017, 224: 262-269.
[18] Long Y, Li B, Liu H. Analysis of fluoroquinolones antibiotic residue in feed matrices using terahertz spectroscopy[J]. Applied Optics, 2018, 57(3): 544-550.
李桂琳, 邓琥, 刘泉澄, 郭志成, 张祺, 尚丽平. 甲硝唑的太赫兹特征吸收光谱分析[J]. 激光与光电子学进展, 2020, 57(17): 173001. Guilin Li, Hu Deng, Quancheng Liu, Zhicheng Guo, Qi Zhang, Liping Shang. Terahertz Characteristic Absorption Spectral Analysis of Metronidazole[J]. Laser & Optoelectronics Progress, 2020, 57(17): 173001.







