Zeta电位计算过程中Henry函数的优化表达式  下载: 837次
下载: 837次
1 引言
分散在液体中的颗粒做电泳运动时,固定吸附层和部分溶剂分子会随之一起移动,与液体之间形成滑动面,定义滑动面与液体内部的电位差为Zeta电位[1]。Zeta电位是衡量胶体稳定性的重要参数,其绝对值越高,表明颗粒间的静电排斥力越大,胶体越稳定;反之,胶体越不稳定。因此,Zeta电位的测量对确定和调节胶体系统的稳定性具有重要意义。但滑动面是一个假想面,Zeta电位无法直接测量,使用电泳光散射的方法,可以测量出带电颗粒在电场中的电泳速度,进而计算出其电泳迁移率[2]。研究表明,颗粒的Zeta电位与其电泳迁移率间存在着正比例关系,比例系数为Henry函数,只有确定了Henry函数的数值,才可以计算出确切的颗粒Zeta电位,因此,准确确定Henry函数对测量Zeta电位极其重要。
1921年,von Smoluchowski[3]考虑了电渗,假设电场均匀且平行于颗粒表面,双电层厚度远远小于颗粒的半径,即
本文利用最小二乘算法对精确Henry函数值进行拟合,获得优化Henry函数表达式,并在Gouy-Chapman-Stern双电层模型[10]的基础上,给出双电层厚度的计算方法,从而获得准确的
2 Henry函数的优化近似表达式
电泳光散射方法测量颗粒的电泳速度后,电泳迁移率可以通过电泳速度计算出来,而Zeta电位的计算与双电层模型有关,选择的双电层模型不同,计算得到的Zeta电位就不同。应用Gouy-Chapman-Stern双电层模型进行分析,对于刚性球体颗粒,其电泳迁移率与Zeta电位的关系可表示为
式中
带电颗粒在电场力作用下运动,同时,作用在颗粒上的液体黏滞力阻止颗粒运动;颗粒表面双电层中的反离子向着电场力反方向移动,产生电泳阻滞力;电场导致颗粒周围离子氛中心落后于颗粒中心,产生的弛豫效应进一步阻止颗粒的运动[11]。当这4个力处于平衡状态时,颗粒在液体中以恒定速度运动。但是,电泳阻滞力和弛豫效应对双电层厚度的影响难以准确确定,也导致Henry函数无法准确确定。
Henry[5]根据颗粒使电场变形的条件,给出了Henry函数的分段表达式
式中
当
当
一般情况下,被测颗粒的
为了解决这一问题,Wiersema等[7]根据Gouy-Chapman-Stern双电层模型以及颗粒在溶液中的受力情况,推导了颗粒电泳迁移率和Zeta电位的精确微分方程,得到精确的Henry函数值
式中
式中
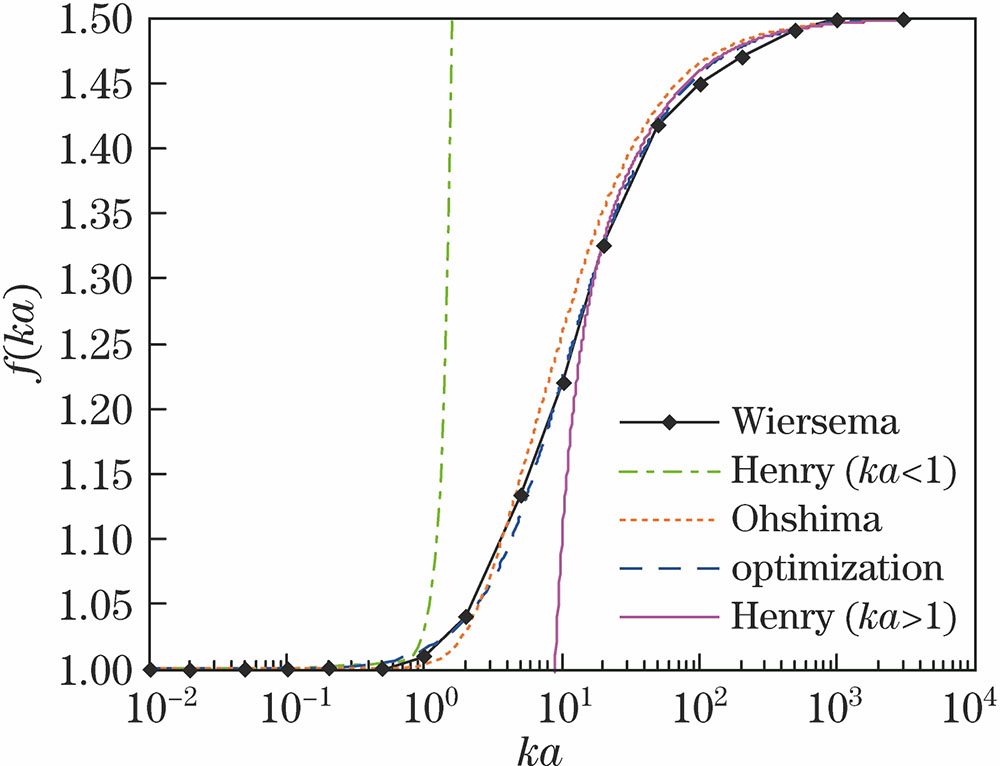
由
表 1. 不同Henry函数的误差对比
Table 1. Comparison of the errors of different Henry functions
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
由
3 参数ka的确定
依据优化Henry函数计算
式中
式中
式中
表 2. 不同电解质类型的离子强度表达式
Table 2. Expressions of ionic strength for different types of electrolyte
|
由于带电颗粒不溶解于电解质溶液,故计算离子强度时的离子不包括带电颗粒本身。
表 3. 不同浓度、不同类型电解质对应的双电层厚度
Table 3. Double layer thickness of different concentrations and different types of electrolyte
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
由
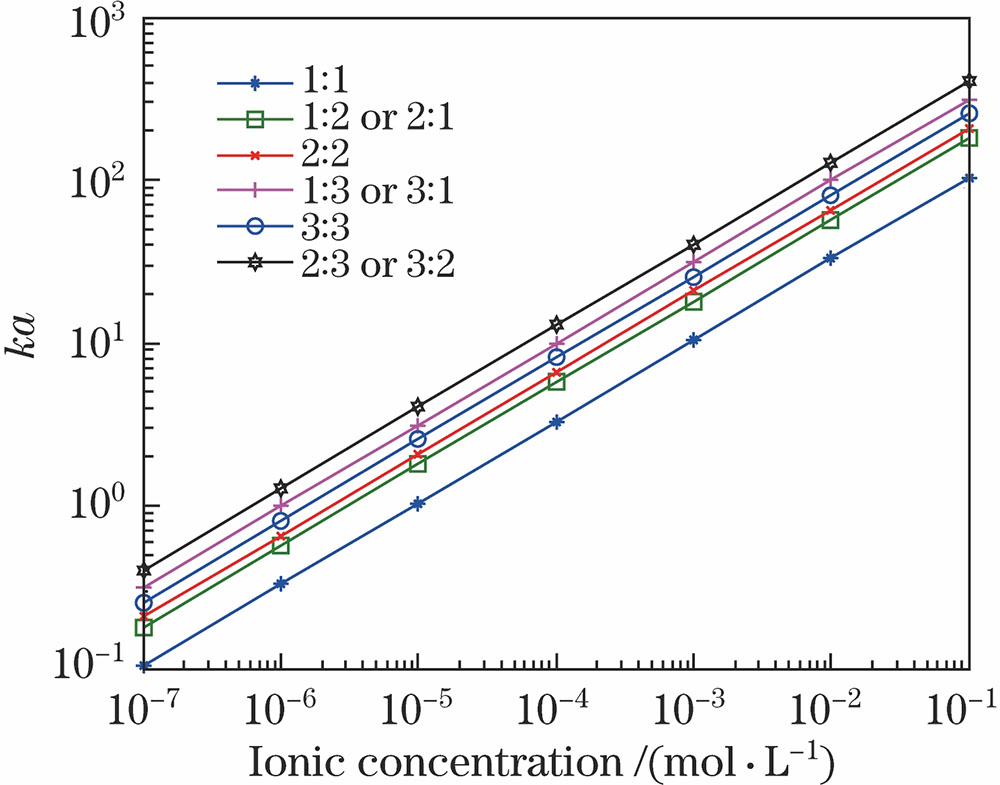
图 2. 不同浓度、不同电解质类型下的球形颗粒对应的ka曲线
Fig. 2. ka curves for spherical particles of different concentrations and different types of electrolyte
由
4 实验与数据分析
4.1 待测样品的制备
将质量为745,74.5,7.45 mg的KCl溶解后分别转移到100 mL容量瓶中,再分别加入0.02 mL质量分数为10%的聚苯乙烯乳胶球标准颗粒(5020A,Duke,美国)后加水定容,配置聚苯乙烯乳胶球体积质量为0.02 mg·mL-1,KCl电解质浓度分别为10-1,10-2,10-3 mol·L-1的样品,编号分别为1、2、3。再配置一个体积为100 mL、分散在超纯水中、体积质量为0.02 mg·mL-1的聚苯乙烯乳胶球样品,编号为4。配制样品时必须用超纯水,避免溶液中出现Ca2+、Ba2+等杂质而影响双电层的厚度。
4.2 Henry函数的计算
依据
因此,编号为1、2、3的样品中带电颗粒的双电层厚度分别为0.962,3.04,9.62 nm,编号为4的样品中带电颗粒的双电层厚度为962 nm。
以1号样品为例,温度为25 ℃时,测得水的黏度为0.8937×10-3 Pa·s,KCl溶液的黏度为0.8854×10-3 Pa·s,相对介电常数为78.5,真空中介电常数为8.854×10-12 F·m-1,玻尔兹曼常数为1.38×10-23,样品中离子强度为
使用纳米粒度仪测得5020A聚苯乙烯颗粒的粒径为203 nm,则颗粒半径与双电层厚度之比为
利用三次样条曲线插值算法,对Wiersema提供的Henry函数值进行插值,当
根据(6)式求得优化Henry函数值为
依据上述方法,得到所有样品的不同Henry函数值,如
表 4. 待测样品的Henry函数值
Table 4. Henry function for the samples to be measured
|
4.3 Zeta电位的测量
利用
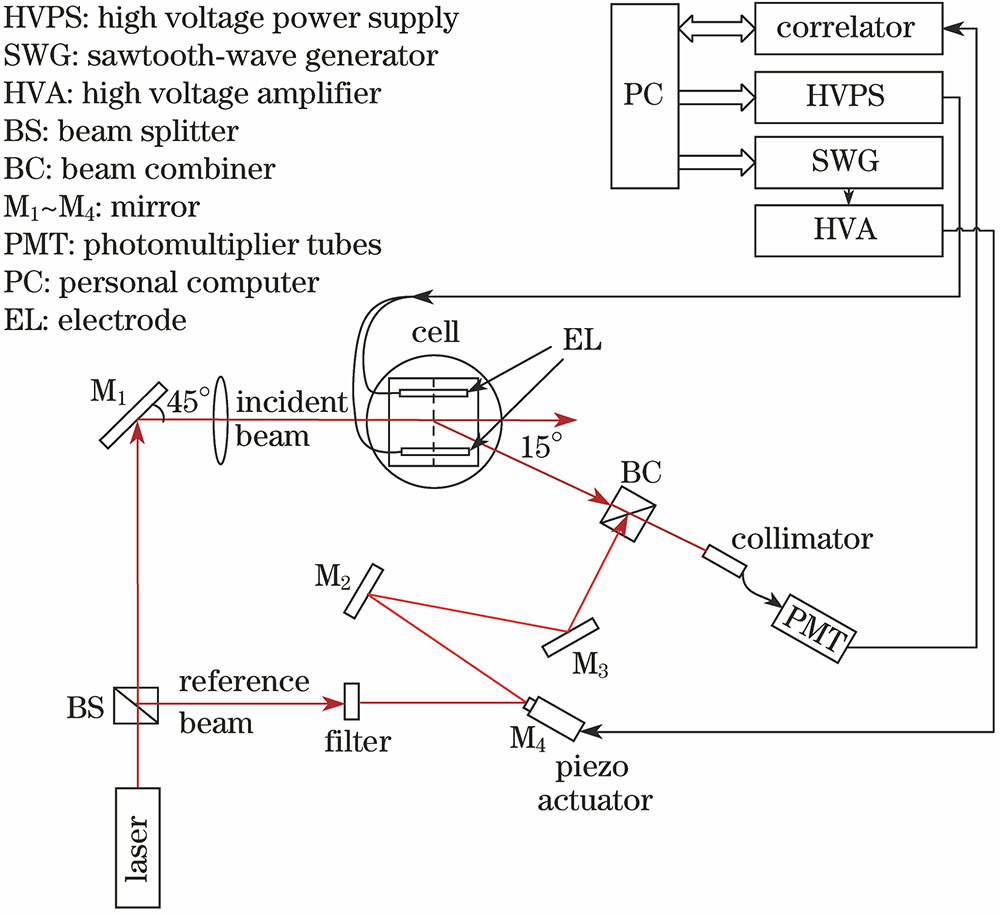
图 3. 电泳光散射法测量装置结构图
Fig. 3. Schematic of the electrophoretic light scattering experiment setup
以1号样品为例,
依据Ohshima推导的近似Henry函数值
表 5. 采用不同Henry函数时颗粒Zeta电位值的比较
Table 5. Comparison of Zeta potentials calculated by different Henry functions
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
由实验结果可以看出,随着电解质溶液浓度的升高,其颗粒电泳迁移率和Zeta电位逐渐减小。通过优化Henry函数计算得到的颗粒Zeta电位值,与Ohshima推导的近似Henry函数计算的颗粒Zeta电位值相比,相对误差由大于3.0%减小到小于1.0%,计算结果更加精确。
5 结论
为提高Henry函数的精度,利用最小二乘算法在0.01<
[3] GreatzL. Handbuch der elektrizitat und des magnetismus[M]. Leipzig:1921.
GreatzL. Handbuch der elektrizitat und des magnetismus[M]. Leipzig:1921.
[4] Huckel E. Die kataphorese der kugel[J]. Physik Z, 1924, 25: 204-210.
Huckel E. Die kataphorese der kugel[J]. Physik Z, 1924, 25: 204-210.
[5] Henry DC. The cataphoresis of suspended particles. Part Ⅰ. The equation of cataphoresis[C]. Proceedings of the Royal Society of London, A: Mathematical, Physical and Engineering Sciences. The Royal Society, 1931, 133( 821): 106- 129.
Henry DC. The cataphoresis of suspended particles. Part Ⅰ. The equation of cataphoresis[C]. Proceedings of the Royal Society of London, A: Mathematical, Physical and Engineering Sciences. The Royal Society, 1931, 133( 821): 106- 129.
[6] Overbeek J T G. Quantitative interpretation of the electrophoretic velocity of colloids[J]. Advances in Colloid Science, 1950, 3: 797-823.
Overbeek J T G. Quantitative interpretation of the electrophoretic velocity of colloids[J]. Advances in Colloid Science, 1950, 3: 797-823.
[11] Miller JF. The determination of very small electrophoretic mobilities of dispersions in non-polar media using phase analysis light scattering[D]. Bristol: University of Bristol, 1990.
Miller JF. The determination of very small electrophoretic mobilities of dispersions in non-polar media using phase analysis light scattering[D]. Bristol: University of Bristol, 1990.
[14] Hunter RJ. Zeta potential in colloid science: principles and applications[M]. London: Academic Press, 2013.
Hunter RJ. Zeta potential in colloid science: principles and applications[M]. London: Academic Press, 2013.
[15] 刘伟, 张珊珊, John C. Thomas, 等. 基于频谱细化算法的电泳光散射Zeta电位测量方法[J]. 光学学报, 2017, 37(2): 0229001.
刘伟, 张珊珊, John C. Thomas, 等. 基于频谱细化算法的电泳光散射Zeta电位测量方法[J]. 光学学报, 2017, 37(2): 0229001.
秦福元, 刘伟, 王文静, JohnC.Thomas, 王雅静, 申晋. Zeta电位计算过程中Henry函数的优化表达式[J]. 光学学报, 2017, 37(10): 1029003. Fuyuan Qin, Wei Liu, Wenjing Wang, C. Thomas John, Yajing Wang, Jin Shen. An Optimal Expression for Henry Function for the Calculation of Zeta Potential[J]. Acta Optica Sinica, 2017, 37(10): 1029003.