基于显微镜数字图像的荧光免疫层析定量检测方法  下载: 863次
下载: 863次
1 引言
荧光免疫层析试纸检测技术是基于免疫层析技术发展而来的,该技术用荧光标记抗原或抗体,通过检测荧光强度就可以实现待测物浓度的检测[1-2]。目前,荧光免疫层析定量检测可分为光电检测法和成像式检测法。光电检测法将光电二极管或光电倍增管作为探测器,ESE Quant定量侧向层析检测仪[3-4]是其中最具代表性的设备。这类分析仪利用步进电机带动试纸条运动,并利用扫描镜头对检测试纸进行扫描,然后将光信号转化为电信号,根据输出的电压值计算被测样品的荧光强度[5-7]。成像式检测法是在成像系统后利用CCD获取试纸条的荧光图像[8-10],然后对图像进行处理得到荧光强度信息。2018年,徐笑晗等[11]利用手持显微镜和CCD设计了荧光免疫层析试条成像检测系统,此系统采用算法提取图像中的荧光面积,然后根据图像的平均灰度值推算荧光强度。光电检测法对机械扫描系统稳定性的要求较高,且容易受背景光的影响。成像式检测方法则忽略了系统的光通量损失,并且将彩色图像整体转化为灰度图像,细分度只有256级[12-13],对试纸条最低灵敏度的检测精度有待提高。
本文首先利用荧光显微镜系统对荧光物质进行激发和探测,建立显微系统的光通量损失方程,计算待测荧光到达CCD像面过程中的光通量损失,然后基于CCD像元的光电转化特性提取数字图像的RGB分量并对其进行加权处理,最后拟合了面阵CCD的量子响应速率曲线。通过计算补偿后的RGB分量亮度加权值来确定荧光强度,然后就可以反演出待测物的浓度。
2 光通量损失方程的建立
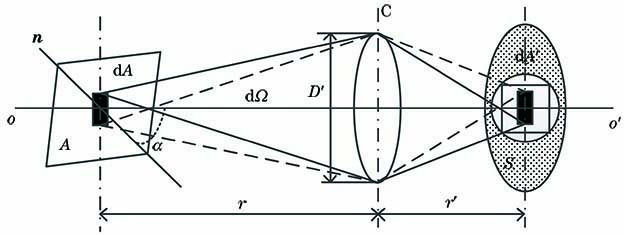
光学系统具有一定的透过率,输出的光通量要比输入的光通量少,光能损失会使光学系统成像的光能量降低。为了获得准确的光强信息,根据几何光学及光度学[14-15]可得到光学成像系统的数学模型,如
当发光面与探测面S不平行时,元发光面的法线n与中心光轴oo'的夹角为α。若元立体角dΩ内发出的光通量为dΦV,则发光面的光亮度LV为
式中:
透镜C与发光面立体角ω之间的关系为
式中:D'为孔径光阑的直径;r为物距。因透镜存在一定的透过率,故而光在传输过程中会产生一定程度的能量损失。根据光的传播规律,探测面S处的光通量ΦV为
式中:τ为透镜C的透过率。由几何关系可得
则探测面dA'的照度EV为
(6)式为光通量损失基本方程。针对荧光显微镜系统的结构特征(发光面与探测面平行,且激发与探测同光路),设计了光学传输模型。根据光通量损失基本方程分析荧光显微系统的光通量损失。
激发光源采用高压汞灯与窄带滤光片的组合,窄带滤光片的中心波长为365 nm,半带宽为10 nm。激发后的荧光经过二向色镜和阻断滤光片后由CCD接收。考虑到荧光显微镜系统中的二向色镜和阻断滤光片都会使光在传输过程中产生一定的损失,根据光通量损失基本方程,建立了荧光显微系统的光通量损失方程,即
式中:EY为CCD像面上接收的照度;L0为荧光亮度;ε为二向色镜的透过率;γ为阻断滤光片的透过率;f为物镜的焦距;l为物镜的物距;fm为物镜的F数。
在进行检测时,系统中的l及f保持不变,则(7)式中的
3 CCD数字图像的处理方法
本文使用维视图像MV-EM510M/C型工业相机采集荧光信息,
面阵CCD的每一个像元都可以看作是一个光电二极管[16]。本文所用工业CCD的像元尺寸为3.45 μm×3.45 μm,有效感光面积为8.5 mm×7.1 mm,可以简单地将其看成是由500万个光电二级管组成的面阵探测器。面阵CCD成像原理如
表 1. CCD相关参数
Table 1. CCD related parameters
|

图 4. 面阵CCD成像原理示意图。(a) CCD成像原理简图;(b) RGB亮度阶梯
Fig. 4. Schematics of area array CCD imaging. (a) Schematic of CCD imaging principle; (b) RGB brightness ladder
维视图像MV-EM510M/C型工业相机的拜耳滤光片以BGGR方式排列,
利用CCD输出的数字图像信息得到原始图像的RGB分量,然后再对每个RGB像元的亮度值进行统计分析。利用MATLAB统计质量浓度为50 ng/mL尿孕酮标准检测样品的数字图像信息后,就可以计算得到RGB像元亮度直方图,如

图 5. RGB像元亮度直方图。(a) R分量像元亮度直方图;(b) G分量像元亮度直方图;(c) B分量像元亮度直方图
Fig. 5. RGB component pixels brightness histogram. (a) R component pixel brightness histogram; (b) G component pixel brightness histogram; (c) B component pixel brightness histogram
为了提升亮度区间范围,将亮度值与像元数做乘积运算,得到RGB分量的亮度加权值,利用加权后的亮度值计算CCD像面上的电子响应亮度值E'Y。通常使用常规色域系统的数字亮度方程描述RGB信号与亮度信号的关系[18],即
式中:E'R、E'G、E'B分别为R、G、B分量的亮度加权值。经计算可知E'R=65.16385×105,E'G=3973.60052×105,E'B=3148.34580×105,从而可以得到CCD像面上的电子响应亮度值E'Y=2170.90190×105。
此外,由于CCD存在一定的量子转化效率,在将光子转化为电子的过程中,接收的光子数和响应的电子数会受到入射波长的影响。为了减小检测误差,需要对CCD像面上的电子响应亮度值进行补偿,其中CCD的量子响应速率曲线如
激发后的荧光的中心波长为615 nm,其对应的量子响应速率接近0.8。拟合量子响应速率曲线后,CCD像面上接收的照度EY为
经计算可知EY=3388.62737×105,将其代入荧光显微系统的光通量损失方程,可求得荧光亮度L0。
4 实验结果及分析
常用的免疫荧光层析法有竞争法和夹心法。竞争法的待检分子浓度与荧光强度呈负相关,而夹心法与竞争法相反,待检分子数越多,激发的荧光越强[19-20]。用竞争法标记的尿孕酮(P)标准样品的荧光免疫反应原理如

图 7. 荧光免疫反应原理。(a)待测溶液的制备;(b)试纸结构
Fig. 7. Principle of fluorescence immunity reaction. (a) Preparation of test solution; (b) structure of test paper
首先需要配制待测溶液,如
表 2. 拟合结果
Table 2. Fitting result
|
激素代谢物(HM)的浓度与荧光亮度之间的关系式为
式中:η0为激素代谢物(HM)的分子数;η为单抗(mAb)的分子数;Ke为发光系数。激素代谢物(HM)的分子数和与之结合的单抗分子数一致,而剩余的单抗分子数可以通过检测T线的荧光亮度获得,因此可以计算得到激素代谢物(HM)的浓度。
第一次实验时,将质量浓度远超100 ng/mL的尿孕酮激素代谢物溶液滴入空白试纸上,C线发光,T线不发光。保持荧光显微镜的光源亮度值恒定,分别检测C线和T线的荧光信号强度,并规定C线和T线的相对荧光信号强度值为100000和0,则激素代谢物(HM)的相对荧光信号强度值在0~100000区间内。
选取12组不同浓度的尿孕酮(P)标准样品滴入空白试纸条上进行检测。根据相对荧光信号强度值与浓度的关系,采用最小二乘法进行线性回归分析,拟合后的数据如

图 8. 不同浓度尿孕酮(P)分子的荧光信号强度曲线
Fig. 8. Fluorescence signal intensity curves of urine progesterone (P) molecule with different mass concentrations
再选取质量浓度为0.5 ng/mL的尿孕酮(P)标准样品,将其滴在空白试纸条上,在检测条件不变的情况下进行12次检测,得到的数据如
检测结果的变异系数(Cv)为
式中:σ(X)表示样本数据的标准差;E(X)表示样本数据的平均值。经计算可知Cv值为3.04%,满足检测标准。
5 结论
本文介绍了基于荧光显微镜数字图像处理的荧光免疫层析定量检测方法。本文首先构建了显微系统的光通量损失方程,然后对提取的RGB分量进行加权处理,增大亮度区间的范围,之后拟合了面阵CCD的量子响应速率曲线,最后获得了荧光强度值,并根据荧光强度反演出了待测物尿孕酮(P)的浓度。经计算可知检测结果的变异系数为3.04%,相关拟合系数大于0.99。
本文检测方法具有较好的重复性和线性拟合度,对荧光检测具有一定的参考价值。
[4] Jin L Z, Jun H, Xiao C L. Comparative study between ABBOTTi2000 automatic luminometer and immone i-CHROMA reader immunofluorescence analyzer in the detection of total prostate-specific antigen[J]. Chinese Journal of New Clinical Medicine, 2011, 4(4): 179-187.
[5] Huang L H, Zhou L, Zhang Y B, et al. A simple optical reader for upconverting phosphor particles captured on lateral flow strip[J]. IEEE Sensors Journal, 2009, 9(10): 1185-1191.
[6] 王燕飞, 余东升, 陈海燕, 等. 便携式MicroRNA快速检测系统[J]. 光学精密工程, 2018, 26(3): 541-547.
[7] 王姗姗, 黄凯, 李铭, 等. 基于BP神经网络的血红蛋白定量光学检测方法[J]. 光学学报, 2018, 38(7): 0717002.
[8] 刘军, 赵吉宾, 刘伟军, 等. 基因芯片荧光靶点阵列图像CCD扫描采集系统[J]. 中国激光, 2010, 37(2): 505-509.
[9] 张球, 梁东, 白丽华, 等. 光片荧光显微镜长时间的稳定成像[J]. 中国激光, 2019, 46(4): 0407001.
[10] Gui C, Wang K, Li C, et al. A CCD-based reader combined with CdS quantum dot-labeled lateral flow strips for ultrasensitive quantitative detection of CagA[J]. Nanoscale Research Letters, 2014, 9(1): 57.
[11] 徐笑晗, 夏果, 金施群, 等. 荧光免疫层析试条成像检测系统的设计[J]. 中国激光, 2018, 45(4): 0407005.
[12] 郑运平, 陈传波. 一种新的灰度图像表示算法研究[J]. 计算机学报, 2010, 33(12): 2397-2406.
Zheng Y P, Chen C B. Study on a new algorithm for gray image representation[J]. Chinese Journal of Computers, 2010, 33(12): 2397-2406.
[13] 冯维, 曲兴华, 王惟婧, 等. 基于数字微镜成像系统的响应曲线标定方法研究[J]. 光学学报, 2018, 38(4): 0411006.
[14] Herzberger M, Chako N. Modern geometrical optics[J]. Physics Today, 1959, 12(6): 50-52.
[15] MaîtreH. Radiometry and photometry[M] //From Photon to Pixel. Hoboken, NJ, USA: John Wiley & Sons, Inc., 2015: 109- 143.
[16] 马骏, 肖喜中, 郎均慰, 等. 航空推扫高光谱成像仪CCD探测器选型研究[J]. 光学学报, 2014, 34(10): 1011001.
[17] Adams J E. Jr. Design of practical color filter array interpolation algorithms for digital cameras[J]. Proceedings of SPIE, 1997, 3028: 117-125.
[18] International TelecommunicationUnion. Recommendation ITU-R: BT.601-7[S]. [S.l.]: Radiocomm-Unication Sector of ITU, 2011.
[19] Chen X J, Xu Y Y, Yu J S, et al. Antigen detection based on background fluorescence quenching immunochromatographic assay[J]. Analytica Chimica Acta, 2014, 841: 44-50.
[20] Arao S, Matsuura S, Nonomura M, et al. Measurement of urinary lactoferrin as a marker of urinary tract infection[J]. Journal of Clinical Microbiology, 1999, 37(3): 553-557.
Article Outline
李婷婷, 冯大伟, 李琦, 向阳, 贾强, 路雨桐, 赵阳. 基于显微镜数字图像的荧光免疫层析定量检测方法[J]. 中国激光, 2020, 47(11): 1107001. Li Tingting, Feng Dawei, Li Qi, Xiang Yang, Jia Qiang, Lu Yutong, Zhao Yang. Quantitative Detection Method of Fluorescence Immunochromatography Based on Microscopic Digital Image[J]. Chinese Journal of Lasers, 2020, 47(11): 1107001.