基于图像局部熵的混合水平集模型甲状旁腺分割  下载: 1069次
下载: 1069次
ing at the characteristics of the intensity inhomogeneous and diversiform parathyroid lesions in the ultrasound images of the parathyroid gland, we propose a hybrid level set model for parathyroid gland segmentation based on local entropy of images. The proposed model uses both global and local image information. To address the problem of the inhomogeneous intensity distribution in ultrasound images,local entropy of images is used to determine the weight of the global term to improve the model’s adaptivity. In addition, two scales are adopted to prevent over-segmentation and calculation inefficiency on the large and small scales, respectively. Experimental results show that the proposed model can adapt to different ultrasound images of parathyroid gland, which makes the evolution curve converge to the target contour automatically. In addition, this model has high segmentation accuracy and computational efficiency.
1 引言
慢性肾病患者体内钙磷代谢紊乱,刺激甲状旁腺激素分泌,诱发甲状旁腺增生,导致继发性甲状旁腺功能亢进[1]。目前超声检查是医生诊断甲状旁腺功能亢进的主要手段,利用超声图像可判断出增生的甲状旁腺位置、数目、形态、内部回声等。超声图像中甲状旁腺病灶的准确分割可以为病情诊断、超声引导下介入手术治疗提供依据,具有显著的临床意义与研究价值。
图像分割方法可分为基于区域的图像分割、基于边缘的图像分割和结合模糊理论、图论、神经网络、水平集等特定理论的图像分割。与基于区域、边缘等传统分割方法相比,基于特定理论的图像分割具有更高的分割精度和稳健性[2]。对于噪声大、组织间边界模糊的超声图像[3],传统分割方法分割边界不连续,无法满足分割目标区域完整性的要求。而且甲状旁腺超声图像中甲状旁腺病灶形态多样,与周围组织对比度低、边界不清晰,传统方法不能准确分割甲状旁腺病灶。而水平集方法对噪声不敏感,它将曲线演化问题转换为偏微分方程求解,把演化曲线嵌入水平集函数中计算分析,可灵活处理曲线的拓扑变化,用闭合的演化曲线描述超声图像中形态各异的组织器官边界,稳定性好、准确度高,在灰度对比度低的图像分割中得到广泛应用[4]。
Chan和Vese提出的CV模型[5-6]利用图像全局信息,能克服传统图像分割方法边界断续、扩展性差的缺点,对目标和背景灰度分布较均匀的图像,分割效果好,且抗噪性好、实现简单。但甲状旁腺体积小且周围有多种其他组织,使得甲状旁腺超声图像背景复杂且灰度分布不均匀,使用CV模型易把其他组织误分为甲状旁腺。Li等[7]提出基于图像局部信息的区域尺度拟合(RSF)模型,该模型利用图像像素点邻域灰度信息,可分割灰度不均匀图像,但易陷入局部极小值,对初始轮廓位置敏感,不能准确分割甲状旁腺病灶。Wang等[8]提出局部区域图像拟合(LGIF)模型,该模型在RSF模型基础上引入全局信息,提高了灰度分布不均匀图像的分割效果,但该模型采用固定权重和固定尺度的邻域窗口,当甲状旁腺病灶毗邻其他组织或边缘较弱时,易出现错分割、过分割,降低了模型的自适应能力。水平集方法一般通过设定迭代次数来停止曲线演化,为保证准确分割目标,需要设定较大的迭代次数,容易出现演化曲线已到达目标轮廓但还需再继续迭代的情况,增加了计算时间。
针对甲状旁腺超声图像灰度分布不均匀、不同患者间差异大的特点,本文利用图像全局和局部信息,提出一种基于图像局部熵的自适应两尺度混合水平集模型,并给出使演化曲线自动收敛于目标轮廓的终止准则,以提高模型的分割准确率和计算效率。
2 水平集模型
2.1 基于全局信息的CV模型
CV模型假设图像由灰度分布均匀的两部分组成,演化曲线C将图像Ω分为目标Ω1和背景Ω2两部分,其能量函数为
式中:I(x,y)为图像的灰度;k=1, 2;c1、c2分别为演化曲线C内外的灰度均值;λk为取值为正的常数;x、y分别为图像的横、纵坐标。
当演化曲线C位于目标轮廓内部或外部时,ECV(C,c1,c2)>0,只有演化曲线C到达目标轮廓时,能量函数最小,即ECV(C,c1,c2)≈0,因此可通过使能量函数最小实现目标分割。根据变分法原理和梯度下降法,用零水平集表示演化曲线C,(1)式的水平集函数演化偏微分方程为
式中:t为时间;ϕ为水平集函数;δε(ϕ)为一维Dirac函数,δε(ϕ)=
文献[
6]为使模型无需重新初始化,加快收敛速度,令λ1=λ2=1,(2)式中平方差可展开成2(c1-c2)
改进CV模型利用全局信息能很好地分割灰度均匀的图像,对初始轮廓位置不敏感,但其对灰度不均匀分布的甲状旁腺超声图像会产生欠分割。
2.2 基于局部信息的RSF模型
RSF模型利用图像局部灰度信息对曲线进行演化,能量函数为
式中:I(y)为点x局部区域内点y处的灰度;Kσ为标准差为σ的高斯函数;f1(x)、f2(x)为点x处的演化曲线内外图像的局部灰度拟合函数。f1(x)、f2(x)的计算公式为
式中:*为卷积运算。根据变分法原理和梯度下降法,(5)式的水平集函数演化偏微分方程为
式中:e1、e2的计算公式为
RSF模型中局部区域的尺度和标准差σ有关,σ取值大,则局部区域尺度大,若甲状旁腺病灶边缘较弱或与血管等组织相连,当演化曲线位于目标轮廓附近时,演化曲线容易“迈过”目标轮廓,出现过分割;σ取值小,局部区域尺度小,这会降低曲线演化速度。RSF模型利用图像局部信息,可分割灰度分布不均匀图像,但对初始轮廓位置敏感,易陷入局部极小值,把其他组织错分为甲状旁腺病灶。
3 基于图像局部熵的自适应两尺度混合水平集模型
由于超声设备以及患者个体的差异,甲状旁腺病灶呈多样化,超声图像中病灶和周围组织边界清晰程度各异,且灰度分布不均匀,单独采用CV模型或RSF模型都不能准确分割甲状旁腺病灶。本文利用CV模型初始轮廓稳健性强和RSF模型可分割灰度分布不均匀图像的优势,提出混合水平集模型,即
式中:α、β分别为全局项和局部项的权重。
为保证演化曲线在演化过程中的光滑和稳定,在混合水平集模型中加入长度项和惩罚项[9],故完整的水平集函数演化偏微分方程为
式中:ν、μ分别为长度项和惩罚项的系数;div为散度。
演化曲线远离目标轮廓或位于灰度分布均匀区域时全局项驱动力很强,使曲线快速向目标轮廓演化;演化曲线位于目标轮廓附近或位于灰度分布不均匀区域时局部项驱动力很强,使曲线准确停靠在目标轮廓上。不同的甲状旁腺超声图像中的初始轮廓到目标轮廓的距离不同,且图像灰度分布不同。当初始轮廓距离目标轮廓较远时,演化曲线可能位于均匀区域,此时应由全局项主导曲线向目标轮廓演化,全局项权重应较大。当初始轮廓在目标轮廓附近时,演化曲线处于非均匀区域,此时应由局部项主导曲线演化,全局项权重应较小。所以对于不同的甲状旁腺超声图像,局部项权重保持不变。当演化曲线远离目标轮廓时,可使全局项权重较大,全局项为主要驱动力;当演化曲线在目标轮廓附近时,可使全局项权重较小,局部项为主要驱动力。
3.1 基于图像局部熵确定全局项权重
对于一幅大小为M×N的灰度图像,设f(i,j)为图像点(i,j)处的灰度值,图像的灰度等级L=256,则图像熵定义为[10]
式中:nl为图像中灰度值为l的像素个数;l=0,1,2,…,255;Pl为图像中像素灰度值为l时的概率。
对图像中任意点(i,j),设其邻域大小为m×n的窗口内灰度值为l的像素个数为n'l,其概率P'l=
和图像熵不同,图像局部熵反映图像中某点局部窗口内的灰度分布均匀性,即局部窗口内灰度等级越多,灰度分布越不均匀,图像局部熵越大,反之图像局部熵越小。
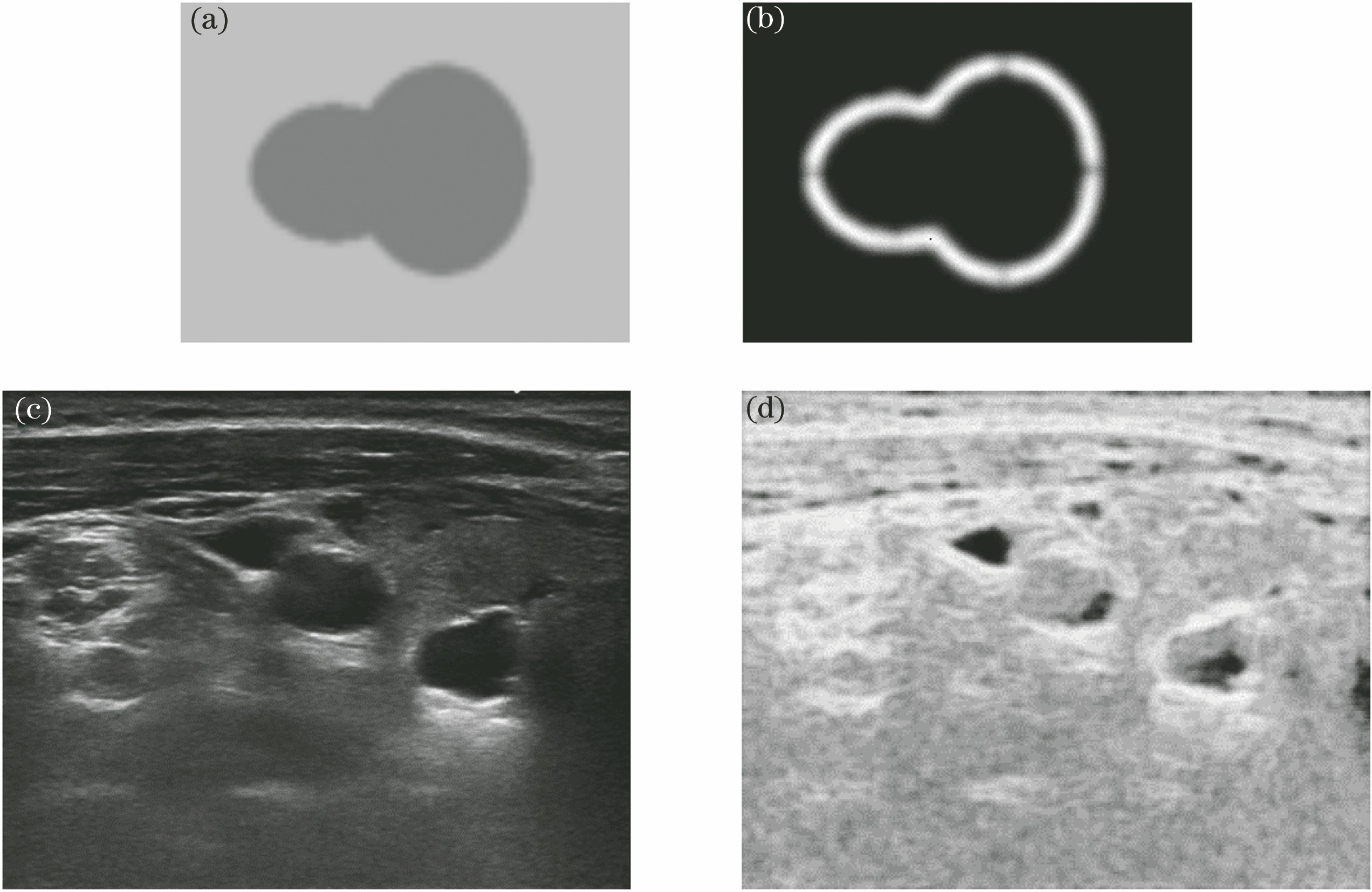
图 1. 灰度分布均匀图像、甲状旁腺超声图像及其对应局部熵图像。(a)灰度分布均匀图像; (b)灰度分布均匀图像的局部熵;(c)甲状旁腺超声图像;(d)甲状旁腺超声图像的局部熵
Fig. 1. Intensity homogeneous image, parathyroid ultrasound image, and their local entropy images. (a) Intensity homogeneous image; (b) local entropy of intensity homogeneous image; (c) parathyroid ultrasound image; (d) local entropy of parathyroid ultrasound image
基于图像局部熵定义混合水平集模型中全局项权重为
式中:矩阵元αij=exp[-h(i,j)],1≤i≤M,1≤j≤N。
由(13)式可知,图像中像素点邻域灰度分布越均匀,该点对应的图像局部熵越小,全局项权重越大;邻域灰度分布越不均匀,该点图像局部熵越大,全局项权重越小。基于图像局部熵可以根据图像灰度分布自适应调整全局项权重,保证演化曲线快速向目标轮廓靠近并准确到达目标轮廓。
![不同全局项权重迭代20次时的演化曲线。(a)原始轮廓;(b) α=0.1;(c) α=0.5;(d) α=0.9;(e) αi,j=exp[-h(i,j)]](/richHtml/gxxb/2019/39/12/1217001/img_2.jpg)
图 2. 不同全局项权重迭代20次时的演化曲线。(a)原始轮廓;(b) α=0.1;(c) α=0.5;(d) α=0.9;(e) αi,j=exp[-h(i,j)]
Fig. 2. Evolution curves for iterations 20 with different global weights. (a) Original contour; (b) α=0.1; (c) α=0.5; (d) α=0.9; (e) αi,j=exp[-h(i,j)]
3.2 局部项的自适应两尺度分割
在混合水平集模型的局部项中引入高斯函数以充分利用图像的局部信息进行准确分割,高斯函数标准差的大小决定了局部区域尺度。当甲状旁腺病灶与周围其他组织相连或病灶和周围组织灰度对比度较低使得目标轮廓边缘较弱时,如果局部区域尺度过大,会出现过分割;而如果局部区域尺度过小,则需要更多的迭代次数演化曲线才能到达目标轮廓附近,计算效率低。
针对上述问题,局部项采用两个区域尺度,当演化曲线远离目标轮廓时,局部项首先采用较大的区域尺度,演化曲线快速接近目标轮廓,当演化曲线位于目标轮廓附近时,为避免过分割,采用较小的区域尺度进行演化。在一定连续迭代次数内,设定演化曲线长度变化阈值[11],通过判断连续两次演化曲线长度变化的绝对值是否小于阈值ξlength1,确定演化曲线是否到达目标轮廓附近,当演化曲线到达目标轮廓附近时,采用小区域尺度演化。与采用固定尺度演化相比,局部项两尺度演化可以避免过分割,减少迭代次数。
3.3 基于图像熵的终止准则
在实际应用中,为准确分割目标,水平集方法预先设定一个较大迭代次数来停止曲线演化。当甲状旁腺病灶边界清晰时,演化曲线可能快速到达目标轮廓但尚未达到设定的迭代次数,此时多余迭代次数使得计算量增加。文献[ 11]中设定演化曲线长度变化阈值作为终止条件,但当甲状旁腺病灶和周围组织界限不清晰时,阈值设定太大,演化曲线未到达目标轮廓就已停止,阈值设定太小,难以达到终止条件,陷入死循环。
实际上当演化曲线到达目标轮廓时,演化曲线内外的图像熵变化很小。因此本文在演化曲线长度变化终止准则基础上,引入图像熵终止条件判据:在一定连续迭代次数内,连续两次演化曲线长度变化小于阈值ξlength2且演化曲线内外的图像熵变化都小于阈值ξentropy时,曲线停止演化。由于加入图像熵的终止条件,演化曲线长度变化阈值可以设定较大,避免陷入死循环,使演化曲线能自动收敛于目标轮廓。
4 实验分析
本文使用Intel(R) Core(TM) i5-4200M CPU 2.5 GHz计算机处理器,选取某医院提供的患者甲状旁腺超声图像,基于Microsoft Visual Studio 2010开发平台和OpenCV2.4.3编程环境,采用本文混合水平集模型进行甲状旁腺病灶分割,并与文献[ 6,12]的水平集模型分割结果进行比较。
混合水平集模型参数设置:局部项权重β=0.05;局部项区域尺度分别为σ1=14,σ2=7;λ1=λ2=1;ε=1;长度项系数ν=0.008×255×255;惩罚项系数μ=1;演化曲线长度变化阈值ξlength1=5,ξlength2=3;图像熵变化阈值ξentropy=0.0001。

图 3. 不同灰度分布甲状旁腺超声图像。(a)(b)边缘清晰的甲状旁腺;(c)有弱边缘的甲状旁腺;(d)(e)边缘模糊的甲状旁腺;(f)与其他组织相连的甲状旁腺
Fig. 3. Parathyroid ultrasound images with different intensity. (a)(b) Parathyroid lesion with clear edge; (c) parathyroid lesion with weak edge; (d)(e) parathyroid lesion with fuzzy edge; (f) parathyroid lesion connected to the other tissue
表 2. 本文模型在不同尺度下分割结果评价
Table 2. Segmentation results of the proposed model at different scales
|
表 1. 不同模型甲状旁腺分割结果评价
Table 1. Parathyroid segmentation results with different models
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
进一步采用骰子相似系数(DSC) [13] 比较不同水平集模型的分割结果,DSC定义为
式中:SS、ST分别为水平集模型分割结果和医生的准确分割结果;∩为交集。DSC的值越接近1,表示分割准确率越高。
![三种水平集模型的甲状旁腺病灶分割结果。(a)含初始轮廓的甲状旁腺感兴趣区域;(b)文献[6]模型分割结果;(c)文献[12]模型分割结果;(d)本文模型分割结果](/richHtml/gxxb/2019/39/12/1217001/img_4.jpg)
图 4. 三种水平集模型的甲状旁腺病灶分割结果。(a)含初始轮廓的甲状旁腺感兴趣区域;(b)文献[ 6]模型分割结果;(c)文献[ 12]模型分割结果;(d)本文模型分割结果
Fig. 4. Segmentation results of different types of parathyroid images by three models. (a) Parathyroid ROI with original contour; (b) segmentation results of the model in Ref. [6]; (c) segmentation results of the model in Ref. [12]; (d) segmentation results of the proposed model
为比较两尺度与单尺度的分割准确率,以

图 5. 本文模型在不同尺度下的分割结果。(a)小尺寸;(b)大尺寸;(c)两尺度
Fig. 5. Segmentation results of the proposed model at different scales. (a) Small scale; (b) large scale; (c) two-scales
5 结论
针对不同个体甲状旁腺超声图像差异大、灰度分布不均匀的难点,提出一种基于图像局部熵的自适应两尺度混合水平集模型。利用图像局部熵自适应确定不同灰度分布图像的全局项权重,提高了模型的自适应能力;利用两尺度方法避免过分割,解决了其他水平集模型分割甲状旁腺病灶时出现的错分割、过分割、计算量大等问题。实验结果表明,本文模型对不同灰度分布的超声图像中甲状旁腺分割有更高的分割准确率和计算效率。
[2] 许新征, 丁世飞, 史忠植, 等. 图像分割的新理论和新方法[J]. 电子学报, 2010, 38(S1): 76-82.
[3] 赵方珍, 梁海英, 巫湘林, 等. 基于局部和全局高斯拟合的主动轮廓分割模型[J]. 激光与光电子学进展, 2017, 54(5): 051006.
[4] 谢志南, 郑东, 陈嘉耀, 等. 改进Chan-Vese模型的肝癌消融CT图像肿块分割方法[J]. 激光与光电子学进展, 2017, 54(2): 021702.
[5] Chan T F, Vese L A. Active contours without edges[J]. IEEE Transactions on Image Processing, 2001, 10(2): 266-277.
[6] 张开华, 周文罡, 张振, 等. 一种改进的C-V主动轮廓模型[J]. 光电工程, 2008, 35(12): 112-116.
[9] SumathiK, MaheshV, RamakrishnanS. Analysis of intima media thickness in ultrasound carotid artery images using level set segmentation without re-initialization[C]∥2014 International Conference on Informatics, Electronics & Vision (ICIEV), May 23-24, 2014, Dhaka, Bangladesh. New York: IEEE, 2014: 15224731.
[12] 周丽芬, 李苹, 任雪利. 一种改进的图像分割活动轮廓模型[J]. 计算机应用与软件, 2013, 30(8): 184-186, 196.
[13] DietenbeckT, AlessandriniM, FribouletD, et al. Creaseg: a free software for the evaluation of image segmentation algorithms based on level-set[C]∥2010 IEEE International Conference on Image Processing, September 26-29, 2010, Hong Kong, China. New York: IEEE, 2010: 665- 668.
Article Outline
毛林, 赵利强, 于明安, 魏莹, 王颖. 基于图像局部熵的混合水平集模型甲状旁腺分割[J]. 光学学报, 2019, 39(12): 1217001. Lin Mao, Liqiang Zhao, Ming’an Yu, Ying Wei, Ying Wang. Hybrid Level Set Model for Parathyroid Gland Segmentation Based on Local Entropy of Images[J]. Acta Optica Sinica, 2019, 39(12): 1217001.






