液态中交叠微球的三维纳米级位置测量方法  下载: 738次
下载: 738次
1 引言
随着光学显微镜技术,荧光蛋白和纳米晶体等光谱技术的发展,实时成像技术已经进展到细胞及分子水平[1]。通过这类技术追踪微米尺度微球获取信息的方法可应用于生物物理学,例如光镊测量和磁镊测量[2-3]。在细胞外微环境中,微球跟踪测量在生命科学中扮演了一个极其重要的角色[4],可用于血液细胞元素间及血管内皮细胞间的相互作用等方面[1]。
近年来,微球位置的跟踪测量方法受到了国内外研究人员的广泛关注[5]。目前对于微球横向位置的跟踪测量,主要方法有Hough变换法(HTM)[6]、质心法[7]、互相关法[8]、梯度法[9]等。这些方法都是根据微球图像的特征来测量的,然而实际测量中由于微球间以及微球与溶液中其他物质的相互作用力,微球与其他物体的交叠现象难以避免[10],导致直接使用传统方法不能识别圆的特征而无法测量其横向位置,不利于实际应用。
雷海等[11]对数字全息法重构强度图进行去卷积运算来消除散斑、离焦等信号的噪声。针对上述问题,本文基于这种方法提出全息重构聚焦法(HRFM),将其与Hough变换法相结合来实现对微球三维位置的测量,即对经同轴数字全息法重构后的聚焦微球强度图像采用Hough变换法测量微球的横向位置,再对横向位置所对应的强度曲线拟合得到其轴向位置。为验证本方法的可行性,首先对单个微球进行了测量,并与传统方法进行对比,结果表明采用本方法得到的测量结果明显优于传统方法。对微球与其他物体的交叠,以两个微球之间的交叠为例进行了测量,结果表明采用本方法可以实现对交叠微球的高分辨力三维位置测量,为其在分子动力学和生命科学领域拓宽了应用范围。
2 测量原理
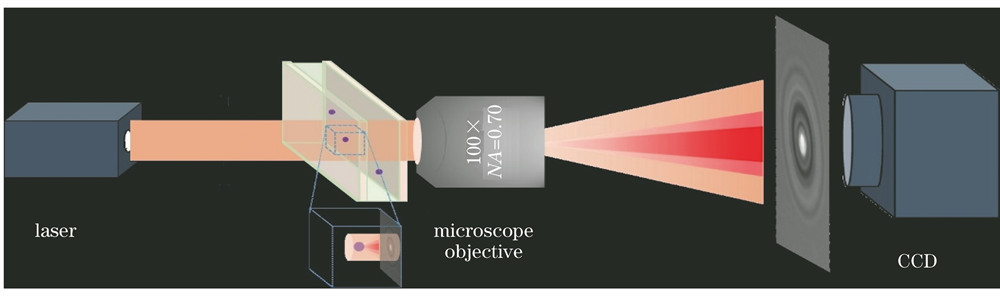
同轴数字全息法的原理为,激光器发出平行光照射微球样品,经微球衍射的光作为衍射光,直接透过的光作为透射光。衍射光和透射光在物镜焦平面处发生干涉形成全息图,经物镜放大后被电荷耦合器件(CCD)相机接收。令衍射光和透射光分别为
衍射光在传播时会逐渐变弱,到达焦平面时会有
式中
式中
式中
式中FFT表示傅里叶变换,
1) 对系统采集的全息图进行减背景和归一化处理并进行重构的衍射计算;
2) 对重构所得强度图进行去卷积运算,消除散斑、离焦等噪声;
3) 根据所得的强度图得到其最大值分布曲线,找到微球聚焦位置;
4) 对微球聚焦位置的强度图采用Hough变换法,得到微球球心横向位置;
5) 对微球球心对应的强度曲线进行多项式拟合,得到微球轴向位置信息[11]。
3 实验装置
实验装置如
系统中使用激光二极管光源(Edmund Optics,#39-569),波长为(670±10) nm。使用的显微物镜(Nikon, CFI L Plan EPI SLWD)放大倍率为100倍,数值孔径
4 实验结果与分析
4.1 单个微球实验

图 2. (a)单个微球的全息图;(b)归一化后的单个微球全息图;(c)单个微球重构后的聚焦图像
Fig. 2. (a) Hologram of single particle; (b) normalized hologram of single particle; (c) focused image after reconstruction of single particle
为验证该算法的可行性,对5 μm直径聚苯乙烯微球样品进行纳米级的阶跃操控,并对采用该算法和传统方法所得结果进行对比。利用三维纳米位移台驱动样品分别在横向和轴向做周期阶跃移动,并采用传统方法和全息重构聚焦法对其分别进行跟踪测量。利用

图 3. 对单个微球采用(a) Hough变换法和(b)全息重构聚焦法测得的横向阶跃位移
Fig. 3. Horizontal step displacement measured by (a) Hough transform method and (b) holographic reconstruction focusing method for single particle
4.2 交叠微球实验
对交叠微球进行测量,采集到的图像如

图 5. (a)交叠微球的全息图;(b)归一化后的交叠微球全息图;(c)交叠微球重构后的聚焦图像
Fig. 5. (a) Hologram of overlapped particles; (b) normalized hologram of overlapped particles; (c) focused image after reconstruction of overlapped particles
5 结论
本文提出了一种全息重构聚焦法,并将其应用于微球三维位置的测量中。对单个微球的测量,相较于传统方法,该方法对重构所得强度图进行去卷积运算,消除一部分噪声,使强度信息更加集中,从而能够更加精确地测量微球的横向位置。对于交叠的微球图像,经重构后也被成功地分离,从而实现对其定位。实验结果表明,此方法可以解决交叠微球位置测量的问题,对单个微球和交叠微球的测量都达到了2 nm的三维位移分辨力,为实现高准确性大通量微球三维位置并行测量提供了可能。
[2] 沈轶. 平行大通量单分子磁力谱方法构建与生物学应用[D]. 上海: 中国科学院上海应用物理研究所, 2012: 38- 45.
沈轶. 平行大通量单分子磁力谱方法构建与生物学应用[D]. 上海: 中国科学院上海应用物理研究所, 2012: 38- 45.
ShenYi. High-through single-molecule magnetic force spectroscope: construction & biological application[D]. Shanghai: Shanghai Institute of Applied Physics,Chinese Academy of Sciences, 2012: 38- 45.
ShenYi. High-through single-molecule magnetic force spectroscope: construction & biological application[D]. Shanghai: Shanghai Institute of Applied Physics,Chinese Academy of Sciences, 2012: 38- 45.
[6] 吕且妮, 高岩, 葛宝臻, 等. 基于霍夫变换的数字全息粒子尺寸测量[J]. 中国激光, 2009, 36(4): 940-944.
吕且妮, 高岩, 葛宝臻, 等. 基于霍夫变换的数字全息粒子尺寸测量[J]. 中国激光, 2009, 36(4): 940-944.
Lü Qieni, Gao Yan, Ge Baozhen, et al. Digital holographic particle sizing with Hough transform[J]. Chinese J Lasers, 2009, 36(4): 940-944.
[7] Arines J, Ares J. Minimum variance centroid thresholding[J]. Optics Letters, 2002, 27(7): 497-499.
Arines J, Ares J. Minimum variance centroid thresholding[J]. Optics Letters, 2002, 27(7): 497-499.
[8] 谢湘军, 雷海, 常新宇, 等. 离焦图像的互相关匹配法测量微球三维位置研究[J]. 光学学报, 2015, 35(2): 0212002.
谢湘军, 雷海, 常新宇, 等. 离焦图像的互相关匹配法测量微球三维位置研究[J]. 光学学报, 2015, 35(2): 0212002.
[11] 雷海, 常新宇, 谢湘军, 等. 去卷积数字全息重构的微球位置精确测量[J]. 光学学报, 2015, 35(4): 0409001.
雷海, 常新宇, 谢湘军, 等. 去卷积数字全息重构的微球位置精确测量[J]. 光学学报, 2015, 35(4): 0409001.
Article Outline
常新宇, 曾雅楠, 雷海, 姚成文, 卢钧胜, 胡晓东. 液态中交叠微球的三维纳米级位置测量方法[J]. 光学学报, 2017, 37(8): 0812002. Xinyu Chang, Yanan Zeng, Hai Lei, Chengwen Yao, Junsheng Lu, Xiaodong Hu. Three-Dimensional Position Measurement Method with Nanoscale Precision for Overlapped Particles in Liquid[J]. Acta Optica Sinica, 2017, 37(8): 0812002.