受激拉曼散射光谱中泵浦光偏振效应的研究
0 引言
相干拉曼散射 (CRS) 是一种基于四波混频的非线性光学过程, 其本质是光场与物质三阶非线性极化率χ(3)之间的相互作用。与自发拉曼散射不同, 相干拉曼散射经常使用两束光场 (泵浦光ωp和Stokes光ωs)。当两束光的频率差等于分子的某一具有拉曼活性的振动频率ωR时, 相干拉曼散射过程发生。随着激光技术的快速发展, 特别是皮秒、飞秒激光的相继出现, 相干拉曼散射灵敏度得以极大提高。据文献报道[8], 与自发拉曼相比, 相干拉曼散射光的灵敏度可以提高104~106个数量级, 这使对介质的快速响应成为可能。由于高的灵敏度以及振动选择性, 相干拉曼散射在生命科学和生物医学成像领域取得长足的发展, 相关研究成果不断涌现[1-3]。
除了高的灵敏度, 激发光的偏振态为调控相干拉曼散射过程提供了一个额外的自由度, 因为介质的三阶非线性极化率χ(3)是一个由81个张量元组成的四阶张量, 其张量元描述了分子对入射激光场偏振态的响应方式。通过组合泵浦光场和Stoke光场的偏振态, 可以选择性地激发分子的某一个或几个张量元, 从而获取分子对称性以及空间取向等信息。
基于相干拉曼散射而发展的非线性光谱技术主要包括相干反斯托克斯拉曼散射 (CARS) 和受激拉曼散射 (SRS) [4]。尽管CARS和SRS同属相干拉曼光谱技术, 但与CARS相比, SRS具有不受三阶非线性极化率中非共振项干扰的优点, 因而所得光谱的峰形与自发拉曼散射完全一致, 不存在光谱失真现象。此外, CARS的信号强度与被测分子浓度的二次方成正比, 而SRS的信号强度与分子浓度的一次方成正比, 这使得SRS在定量分析上具有优势。基于这些优点, SRS不断获得研究者们的青睐, 被广泛用于精密测量、材料科学以及生物工程等领域[5-7], 特别是作为一种新兴的成像技术, SRS显微术在无标记生物体成像领域取得了极大成功, 其中最为典型的是谢晓亮研究组和程继新研究组的工作[2,8-12]。
SRS技术的兴起也促进了对其偏振应用的研究[13-16]。例如, 利用双偏振高光谱SRS显微镜, Shou等[13]实现了在没有偏振调制的情况下同时成像三阶非线性极化率的两个不同分量。2021年, 程继新课题组利用偏振敏感的SRS成像技术揭示了念珠菌膜上两性霉素B的空间取向[16]。不过, 与CARS技术相比, SRS的偏振效应研究还不够充分, 例如没有有关圆偏振的SRS报道; 而对于CARS, 最近的研究结果表明, 圆偏振泵浦光不仅有助于消除CARS非共振背景, 而且还可以调控CARS的信号强度并对分子的对称性进行直接成像 [17,18]。
为此, 本文从理论和实验上开展了泵浦光为圆偏振的SRS研究 (Stokes光仍为线偏振), 并与两束光均为线偏振时的SRS信号进行了对比。
1 理论背景
与CARS类似, SRS也可以被视作四波混频过程, 二者的示意图如
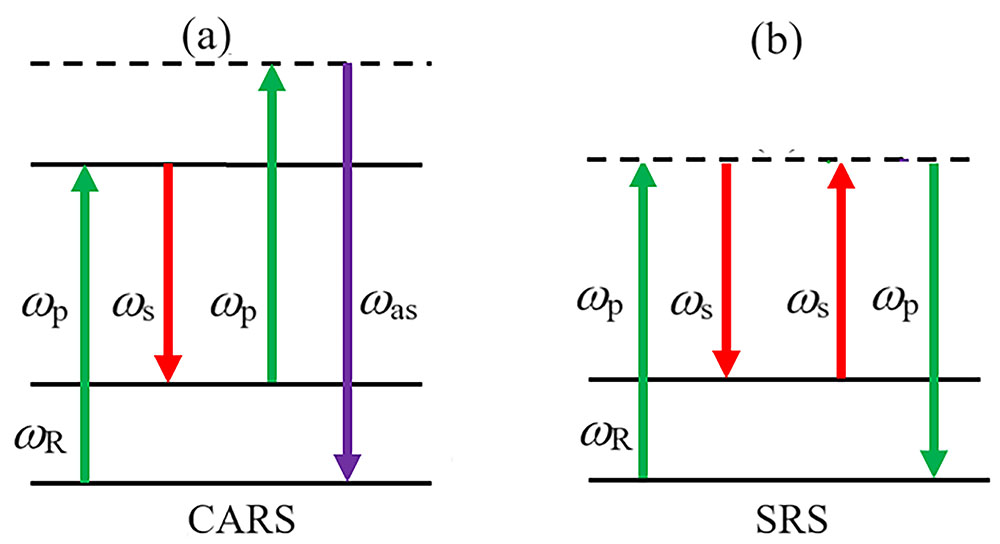
图 1. (a) CARS能级示意图, 其中ωp为泵浦光的频率, ωs为Stokes光的频率, ωas=2ωp-ωs为anti-Stokes频率,ωR为分子的振动频率; (b) SRS能级示意图
Fig. 1. (a) Energy diagram of CARS, where ωp is frequency of pump light, ωs is frequency of Stokes light,ωas is the anti-Stokes frequency at 2ωp-ωs and ωR is molecular vibrational frequency; (b) The energy diagram of SRS
对于如
式中:
对各向同性介质, 三阶非线性极化81个张量元只有21个不恒为0, 且满足如下关系[19]
当泵浦光和Stokes光均为线偏振, 且偏振方向之间夹角为θ 时, 如

图 2. (a) 泵浦光和Stokes光均为线偏振时的矢量图。
Fig. 2. (a) Polarization figure of pump and Stokes beams for linear polarization.
将 (7) 和 (8) 式代入 (1) 式, 得到
假定泵浦和Stokes光场均为沿z方向传播的平面波, 在慢振幅近似下, 耦合波方程为[20]
式中: μ0为真空磁导率, ks为Stokes光的波矢。将 (10) 式对
式中E(ωs, 0) 为最初的Stokes光场。三阶非线性极化率包含非共振项和共振项, 而共振项又包括实部和虚部, 即
式中: ΓR为振动能级ωR的线宽, N为分子的数密度, σ为分子的拉曼散射截面。将 (12) 式代入 (11) 式, 可以得到传播距离为L处的Stokes光强为
式中
式中
类似地, 当泵浦光为圆偏振而Stokes光仍保持线偏振时, 如
由 (14) 和 (17) 式可以看出, SRS的信号强度不仅依赖于泵浦光的偏振态, 还与分子某个特定振动模式的退偏比ρ有关。在拉曼光谱中, 退偏比是一个表征分子振动模式对称性的物理量, 其值范围为0到3/4之间。对于各向同性介质, 如气体和液体等, 当0 ≤ ρ <3/4时, 称之为全对称的振动模, 或偏振模; 一般地, 由于高的对称性, 偏振模的退偏比值接近于0。当ρ = 3/4时, 称之为非全对称的振动模, 或退偏模。通过退偏比的值, 可以判断分子振动模式的对称性, 并据此指认所测量的拉曼光谱。对于各向异性介质, 退偏比可以大于3/4, 甚至大于1 [20]。
2 实验装置
如前所述, SRS过程的发生除了导致泵浦光光强减弱和Stokes光光强增强外, 还将导致振动基态上的分子被激发至振动激发态, 而位于振动激发态上的分子是不稳定的, 将通过与周围其他分子碰撞的方式弛豫回到振动基态, 并将振动激发能转化为分子的平动能, 导致分子内部局部温度升高, 形成压力波, 用一个灵敏的麦克风即可以检测这种波动变化, 得到SRS光谱, 称这种检测方式为受激拉曼光声光谱 (PARS)。由于PARS探测光信号转化为声信号的灵敏度高, 因此本研究设计PARS实验装置来采集信号, 如

图 3. (a) 偏振的PARS实验装置; (b) 单束泵浦光、单束Stokes光以及双束光共同作用下的光声信号,图中光声信号是在两束光偏振相互平行条件下采集的
Fig. 3. (a) Experimental setup for polarized PARS; (b) Photoacoustic signal under the action of single pump beam, single Stokes beam and the two beams, in which the photoacoustic signal is obtained under the condition of parallel polarizations of the two beams
如
如
需要特别说明的是,
为测量SRS的偏振特性, 泵浦光和Stokes光首先经格兰-泰勒棱镜P1和P2 (消光比 < 10-6) 作用以成为高纯度的线偏振光。当测量两束光均为线偏振的SRS光谱时, 如
3 实验结果与讨论
甲烷分子是一种高度对称的球陀螺分子。在C-H伸缩振动区域 (2800~3100 cm-1), 它有两个不同的伸缩振动频率, 全对称的υ1模 (2917 cm-1) 和非全对称的υ3模 (3020 cm-1)。理论上可以严格证明υ1模和υ3模的退偏比ρ分别为0和3/4。因此, 甲烷分子是一个可以用来研究泵浦光偏振态对SRS信号强度影响的理想模型体系。

图 4. 甲烷分子SRS强度随泵浦光和Stokes光偏振方向夹角θ的变化情况。(a) υ1模; (b) υ3模
Fig. 4. Dependence of SRS intensity on the polarization cross angle θ between pump and Stokes beams for CH4 molecule.(a) υ1 mode; (b) υ3 mode

图 5. 不同偏振情形下甲烷分子υ1和υ3模的SRS光谱。(a) 泵浦光和Stokes光线偏振方向相互垂直;(b) 泵浦光和Stokes光线偏振方向相互平行; (c) 泵浦光为圆偏振而Stokes光为线偏振
Fig. 5. SRS spectra of υ1 and υ3 vibrational modes of CH4 under different polarization conditions. (a) Polarizations of pump and Stokes beams are perpendicular to each other; (b) Polarizations of pump and Stokes beams are parallel to each other; (c) Circular polarization of pump beam and linear polarization of Stokes beam
需要说明的是, 不同于红外光谱, 一般情况下, 各向同性介质中, 对称振动模的拉曼光谱强度远大于反对称振动模的拉曼光谱强度, 这一点可以从
此外, 按照 (14) 和 (17) 式, 圆偏振泵浦光的SRS与两束光均为平行线偏振的SRS的强度比为
与线偏振光相比, 圆偏振泵浦光还具有不依赖于样品分子取向、无需找到相对于样品分子的最佳偏振耦合方向来激发样品的优点, 因此圆偏振泵浦光的SRS适合对晶体或生物样品等各向异性样品的检测或成像。另一方面, 圆偏振泵浦光的SRS还可能适合对手性样品分子的分析。拉曼光学活性光谱 (ROA) 是指手性分子在右旋和左旋圆偏振光激发下的自发拉曼光强度差, 蕴藏丰富的分子结构信息。但通常, ROA光谱的强度比较低, 而且容易受荧光的干扰。圆偏振泵浦光和线偏振Stokes光组合的SRS有可能提高ROA光谱的检测灵敏度, 将在未来的实验中做进一步的尝试。
4 结论
受激拉曼散射是近年来迅猛发展的一种非线性光学技术。由于SRS对入射激光场的偏振态非常敏感, 因此操控入射光场的偏振态为扩大SRS技术的应用范围提供了可能性。本研究从理论和实验两个方面对比研究了泵浦光为圆偏振和线偏振情形下的SRS过程 (Stokes光始终保持线偏振)。基于非线性耦合波方程, 给出了上述偏振情形下SRS信号强度与光场偏振态以及分子振动模式对称性之间的依赖关系; 并以甲烷分子为例, 实验上测量了不同偏振情形下υ1和υ3模的SRS光谱, 实验结果与理论分析基本一致。结果表明, SRS的信号强度不仅与泵浦光的偏振态有关系, 还与分子振动模式的对称性紧密相关。通过改变泵浦光的偏振态, 可以改变不同对称性振动模式之间的相对强度。本研究有助于依据分子振动模式对称性来调控SRS信号强度, 改善SRS成像对照水平, 并为SRS技术的偏振应用提供启示。
[1] Li Y P, Shen B L, Li S W, et al. Review of stimulated Raman scattering microscopy techniques and applications in the biosciences[J]. Advanced Biology, 2021, 5(1): e2000184.
[2] Chen W W, Lemieux G A, Camp C H, et al. Spectroscopic coherent Raman imaging of Caenorhabditis elegans reveals lipid particle diversity[J]. Nature Chemical Biology, 2020, 16(10): 1087-1095.
[3] Zhang C, Cheng J X. Perspective: Coherent Raman scattering microscopy, the future is bright[J]. APL Photonics, 2018, 3(9): 090901.
[4] Freudiger C W, Roeffaers M B J, Zhang X, et al. Optical heterodyne-detected Raman-induced Kerr effect (OHD-RIKE) microscopy[J]. The Journal of Physical Chemistry B, 2011, 115(18): 5574-5581.
[5] 鲁思滨, 陈红辉, 陆泽茜, 等. 受激拉曼绝热捷径提高原子干涉仪稳健性的实验研究[J]. 量子电子学报, 2019, 36(4): 434-439.
[6] Cheng Q, Miao Y P, Wild J, et al. Emerging applications of stimulated Raman scattering microscopy in materials science[J]. Matter, 2021, 4(5): 1460-1483.
[7] 王 莹, 刘晓枫, 任盼盼, 等. 共振增强水分子O-H伸缩振动受激拉曼散射[J]. 量子电子学报, 2021, 38(6): 774-779.
[8] Freudiger C W, Min W, Saar B G, et al. Label-free biomedical imaging with high sensitivity by stimulated Raman scattering microscopy[J]. Science, 2008, 322(5909): 1857-1861.
[9] Cheng J X, Xie X S. Vibrational spectroscopic imaging of living systems: An emerging platform for biology and medicine[J]. Science, 2015, 350(6264): aaa8870.
[10] Ji M B, Arbel M, Zhang L L, et al. Label-free imaging of amyloid plaques in Alzheimer's disease with stimulated Raman scattering microscopy[J]. Science Advances, 2018, 4(11): eaat7715.
[11] Zong C, Premasiri R, Lin H N, et al. Plasmon-enhanced stimulated Raman scattering microscopy with single-molecule detection sensitivity[J]. Nature Communications, 2019, 10: 5318.
[12] Ao J P, Fang X F, Miao X C, et al. Switchable stimulated Raman scattering microscopy with photochromic vibrational probes[J]. Nature Communications, 2021, 12: 3089.
[13] Shou J W, Ozeki Y. Dual-polarization hyperspectral stimulated Raman scattering microscopy[J]. Applied Physics Letters, 2018, 113(3): 033701.
[14] Hofer M, Balla N K, Brasselet S. High-speed polarization-resolved coherent Raman scattering imaging[J]. Optica, 2017, 4(7): 795-801.
[15] Munhoz F, Brustlein S, Hostein R, et al. Polarization resolved stimulated Raman scattering: Probing depolarization ratios of liquids[J]. Journal of Raman Spectroscopy, 2012, 43(3): 419-424.
[16] Dong P T, Zong C, Dagher Z, et al. Polarization-sensitive stimulated Raman scattering imaging resolves amphotericin B orientation in Candida membrane[J]. Science Advances, 2021, 7(2): eabd5230.
[17] Upputuri P K, Lin J, Gong L, et al. Circularly polarized coherent anti-Stokes Raman scattering microscopy[J]. Optics Letters, 2013, 38(8): 1262-1264.
[18] Cleff C, Gasecka A, Ferrand P, et al. Direct imaging of molecular symmetry by coherent anti-Stokes Raman scattering[J]. Nature Communications, 2016, 7: 11562.
[19] SutherlR L. Handbook of Nonlinear Optics [M]. 2nd Edition. New York, USA: Marcel Dekker, 2003: 476.
[20] 唐金兰, 包一麟, 吴进锦, 等. 乳腺组织癌变的偏振拉曼光谱学研究[J]. 分析化学, 2021, 49(12): 2048-2054.
Tang J L, Bao Y L, Wu J J, et al. Study on breast tissue cancerization by polarized micro-Raman spectroscopy[J]. Chinese Journal of Analytical Chemistry, 2021, 49(12): 2048-2054.
[21] Yu Y Q, Lin K, Zhou X G, et al. New C⁃H stretching vibrational spectral features in the Raman spectra of gaseous and liquid ethanol[J]. The Journal of Physical Chemistry C, 2007, 111(25): 8971-8978.
[22] Yu Y Q, Wang Y X, Hu N Y, et al. Overlapping spectral features and new assignment of 2-propanol in the C-H stretching region[J]. Journal of Raman Spectroscopy, 2014, 45(3): 259-265.
李涛, 李玉慧, 胡坤, 王盼归, 赵洪辉, 喻远琴. 受激拉曼散射光谱中泵浦光偏振效应的研究[J]. 量子电子学报, 2024, 41(1): 78. Tao LI, Yuhui LI, Kun HU, Pangui WANG, Honghui ZHAO, Yuanqin YU. Polarization effect of pump light in stimulated Raman scattering spectroscopy[J]. Chinese Journal of Quantum Electronics, 2024, 41(1): 78.



