基于时域微分周期比的脉搏波信号特征识别  下载: 563次
下载: 563次
0 引言
血液由心脏有规律地射入主动脉中,动脉血管是一个富有弹性的管路[1],流动的血液使动脉管压力发生变化从而形成脉搏波,其形状周期、各特征长度及峰值等参数蕴含丰富的生理健康信息,与人体心率、动脉硬化程度、血管等健康状况密切相关,研究脉搏波特征信息可以为预防血管疾病提供帮助[2-3].
目前脉搏波检测方式较多的是压电式、光电式、生物电阻抗式等传感器[4],其检测原理基本是由电信号转换而成,因此在特殊医疗环境下[5-6]不可避免地会受到电磁干扰信号的影响,不方便信号采集检测.而在脉搏波研究和特征提取方面,JOAO P C等[7]使用光纤布拉格光栅(Fiber Bragg Grating, FBG)传感器嵌入在PVC载体里检测心脏频率和脉搏波信号,但未提出脉搏特征点的识别.孙薇等[8]用小波变换过零点的方法识别脉搏波特征点,提高了特征提取的准确性,但文中没有对提取重搏波信息进行分析.季忠等[9]用压电式传感器采集脉搏波信号,采用时域特征与小波分解相结合的方法,分析了潮波特征点与小波d5层极值点的对应关系,该方法可以识别潮波和重搏波位置,但是要求原始脉搏波存在容易区分的极值点.但是,由于人体本身和外界的不稳定性,某些潮波和重搏波都隐蔽的情况下没有极值点,或者在特征点附近出现多个极值点,使得部分特征点可能相近或重合,从而不能被准确识别.
为了解决上述方法存在的实际应用范围小或特征点定位不准确的问题,本文采用PDMS封装后FBG柔性传感器,对人体桡动脉处脉搏波信号进行采集,根据潮波和重搏波特征点在脉搏波起点与波峰之间的相对位置,提出了一种改进的微分法——时域微分周期比(Time Domain Differential Ratio, TDDR)的算法来缩小特征定位区间,以提高脉搏特征信息辨别的准确性和适用性.
1 FBG传感器的脉搏波检测
1.1 FBG的应变传感原理
FBG传感器因其灵敏度高、质量轻、耐腐蚀、抗电磁干扰等独特优势[10],已逐步开始应用于医学监测领域.其检测原理是当宽带光源射入光纤传输到光栅时,满足一定波长的光会发生反射,反射波长与其纤芯有效折射率和光栅的周期关系式满足条件
式中,为光纤纤芯有效折射率,为光纤光栅的周期.采集时,因心脏泵血流入动脉,使得手腕桡动脉处表面发生微弱起伏变化,这种变化使FBG反射波长发生漂移.假设外界温度恒定不变,则可通过检测波长的漂移变化量获得脉搏波信号信息,FBG中心波长漂移量与应变变化的关系式为
式中,为有效弹光系数,为应变变化量,为FBG的应变灵敏系数.从式(2)可知FBG作为应变传感器使用时,具有很好的线性输出.
1.2 FBG脉搏波传感器的封装及采集
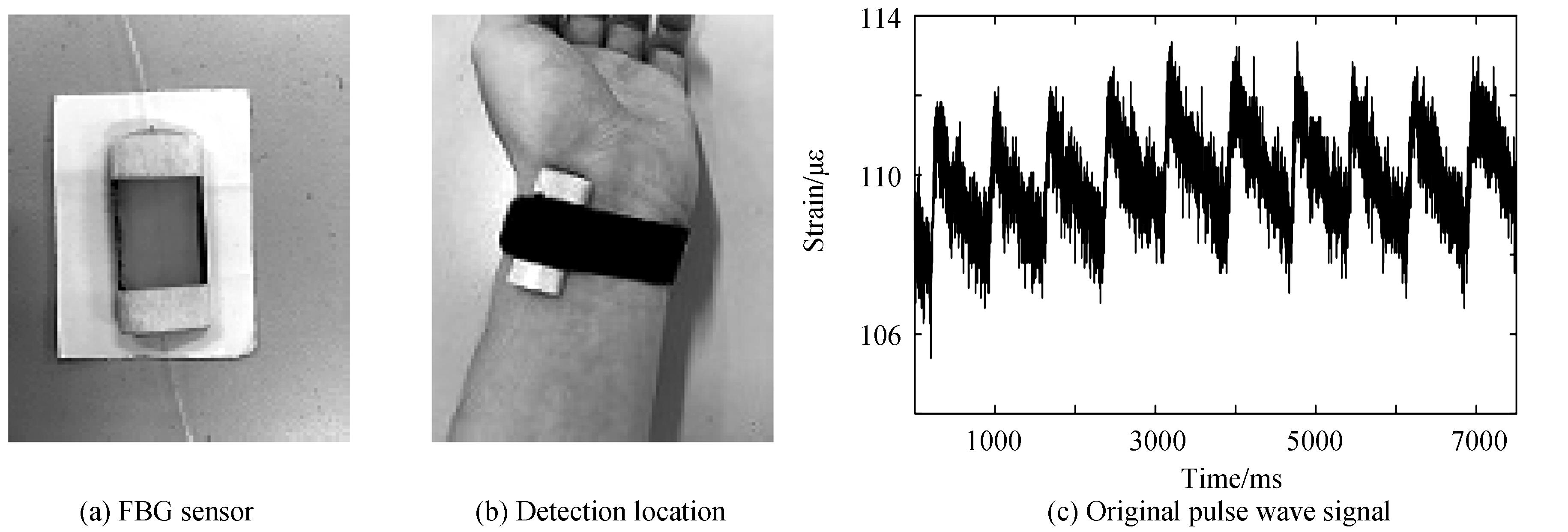
裸FBG在检测脉搏波时,与人体肌肤接触可能存在空隙,且容易受外力破坏传感器结构,影响检测的准确性.采用PDMS封装,厚度为4 mm的FBG柔性传感器[11],能够很好的检测人体脉搏波信号.将A、B两种PDMS溶液按1∶1混合搅拌均匀,FBG纵向放在中间高度位置,待溶液固化后完成封装,制作的柔性传感器如图1(a)所示.将封装好的FBG传感器纵向放置手腕桡动脉处,采用波长解调范围为1 460 nm~1 620 nm,精度为1 pm的MOI-si155进行波长解调,采集频率设置为1 KHz,如图1(b)所示,其中,FBG中心波长为1 544.949 nm,采集数据如图1(c)所示.
2 脉搏波信号预处理及特征划分
2.1 经验模态分解方法预处理
由图1(c)可见,由于脉搏波信号比较微弱,主要能量分布在频率范围内[12],易受到人体自身呼吸和外界工频噪声干扰,信号含有大量噪声并产生相应基线.因此首先需要对信号进行预处理,包括去噪及去基线.
经验模态分解(Empirical Mode Decomposition, EMD)原理是要求给定信号S满足提取模态函数(Intrinsic Mode Function,IMF)的2个基本条件时,从而自适应分解有限个模函数[13-14],每层信号频率由高频到低频,可根据实际需要来提取信号.本文使用MATLAB,对脉搏波信号采用EMD方法自适应分解共12层,如图2所示,逐层分解滤除高频噪声信号和低频基线信号,最后一项为余项层.
从图中不难发现IMF1-IMF6层信号明显含有较高频噪声,而IMF11和res两层频率最低,影响可忽略,因此前6层IMF1-IMF6可视为高频噪声信号,最后2层IMF11,res为基线信号.对IMF7层进行分析,如图3(a)所示,发现频谱主要分布在0~15 Hz之间,符合脉搏波主要能量分布特征.因此剩余其它项叠加即为预处理后的信号,,预处理后信号如图3(b)~(c)所示,信噪比为35.12,已很好地消除脉搏波中的噪声和基线.
2.2 特征点划分及算法流程
在中医临床诊脉中,脉搏波信号主要从桡动脉、股动脉和颈动脉等处获取,一般从这些部位得到的信号,根据其波形形成的机理,在正常生理状态下其特征主要可划分为b、c、d、e、f、g六个阶段,如图4所示.完整的一个脉搏波周期由心室内进入射血状态开始,主动脉压力增加,形成一个总体上升的趋势阶段(b-c段),b为起点,c为波峰点;波峰之后由于心室停止射血,血压下降,动脉内血液回流形成一个反射波形,称为潮波,d、e两点分别为潮波的波谷和波峰;最后心脏收缩再舒张形成重搏波,f、g两点分别为重搏波的波谷和波峰.
从第一个起点b到下一个起点b’整个过程记作一个周期T,从起点b到波峰点c的时间Tc反映了心室射血的快慢,而波峰点的幅值Hc反映了心脏的衰弱情况,潮峰时间Te和幅值He能够反映主动脉压力和血管弹性情况,重搏波峰时间Tg与幅值Hg能够反映心脏功能及血流状态信息.临床医学上通常用反射波增强指数、舒张期增强指数和脉搏波速等参数信息来诊断动脉硬化、心衰等疾病[15-18].为了准确识别起点、波峰点、潮波、重博波的特征信息这些重要特征信息,基于预处理后的脉搏波信号,提出采用基于时域微分周期比(TDDR)的方法,使用MATLAB软件编程,实现从原始脉搏波信号到信号四个特征点的提取,流程图如图5所示.
3 基于时域微分周期比的特征点识别
3.1 起点与波峰的识别
经过预处理后的脉搏波信号,起点和波峰点较明显,也最容易提取识别.为了减小计算量,结合采样频率及脉搏周期平均长度,本文选取长度作为自适应移动识别区间,在此区间求出信号极大值中的最大值,可得到主波峰点c位置;其余波峰点则以前一个波峰点为基点,再加上区间,在此范围内寻找下一个峰值点.为了避免起点误检,在波峰前第一个满足小于三分之一信号均值的极小值点作为起点,记为,整个脉搏周期为,则.
3.2 潮波与重搏波的识别
在脉搏波特征识别过程中,由于人体脉搏的差异,潮波或重搏波特征信息会出现不同的情况,通过大量的脉搏波实验,脉搏波可按特征显隐分为四种类型,分别为潮波和重搏波都明显、潮波隐蔽重搏波明显、潮波明显重搏波隐蔽、潮波和重搏波都隐蔽,对应脉搏波及微分信号如图6(a)~(d)所示,其中图6(e)为特征明显时的特殊情况.
如图6(a)~(b)所示,当重搏波特征点十分明显时,使用文献[5]和文献[6]方法虽然可以识别各特征点,但特征点之间的间距可能过大或过小.如果遇到如图6(c)~(d)所示,在特征点比较隐蔽,没有极值点的情况下;或者如图6(e)所示重搏波(或潮波)微分信号中特征点多次与零线相交,导致周围可能包含多个不易区分的极值点,用上述方法将难以准确识别.由于不同人体的脉搏周期起点到波峰点时间变化差异较大,研究特征点在整个周期的位置会带来不必要的误差,因此本文将波峰点与下一个起点之间的距离记为T1,则,提出通过研究各特征点在T1上的周期比,确定其区间范围,随后在微分信号上对特征点进行定位.
3.2.1 周期比的区间定位
本文分别对10名测试者在静息和运动状态下,连续采集30 s的脉搏波信号并进行预处理,从中选取7名测试者脉搏波,标记每个潮波和重搏波的区间位置,统计其最大最小值,结果如表1所示;最后根据式(3)、(4),分别求出点e、g位于T1的相对位置和.
表 1. 不同状态下潮波与重搏波在T1周期的相对位置
Table 1. The relative position of tidal wave and dicrotic wave in T1 cycle under different conditions
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
从表中可以得出,7名测试者在运动和静息两种状态下,脉搏波周期T1变化范围都较大,可以依据T1的长度来判断测试者的运动状态.同时把不同脉搏波点e、g占比的最大值乘以对应的T1转换为采集点数,经过计算,静息状态下TW和HW分别在波峰后平均150点和340点的位置,考虑到误检和漏检,可适当放大该值,取值为170和390,因此潮波和重搏波特征点分别在微分信号中和区间内寻找;运动状态下特征点之间距离较小,幅值较大,识别区间分别为和,同时该区间对另外3名测试者脉搏波识别也同样适用.
3.2.2 TDDR识别方法
为了避免潮波或重搏波的波峰波谷识别不准确,选取特征点之间距离的平均值β作为最小间距,多次实验发现当β选取为20时,能够有效避免信号中多极值点的干扰,由此,基于各特征信息在脉搏波周期T1中所占的周期比,提出的方法为
1) 潮波、重搏波都明显时:此时微分信号中存在零点和多零点的情况,若特征零点间距明显,则在区间内寻找各特征点对应的零点,如图7(a)所示;若特征点附近存在多零点,如图7(b)所示,则点d或f为较小零点,点e或g为区间内第一个差值大于β的零点.其中“+”表示特征谷点,“x”表示特征峰点.
2) 潮波、重搏波隐蔽时:表示原信号中无零点,则在区间内寻找微分信号中的极大极小值点来判断.实验发现对应区间中,取第一个极大值与左右差值大于β的极小值求平均,能够很好的定位潮波和重搏波的特征点位置,如图7(c),若一阶微分信号中没有极大值点,将该左极小值点与右极限值的区间分为三段,点d、e为分割点;点f和g识别方法相同.
3) 潮波、重搏波单个明显时:如图7(d)~(e)所示,在相对位置区间内分别按明显和隐蔽情况处理.
4 实验结果与分析
选取10位年龄在23~25岁之间健康的测试者在不同状态下的脉搏波各5组,其中男性6名,女性4名,每组采集时间平均30 s.为了验证本文方法的准确性和适用性,分别在静息和运动2种状态下用TDDR法、文献[5]方法、文献[6]方法进行特征定位对比,如图8~9所示,其中“”表示起点,“*”表示波峰点,“+”、“×”分别表示潮波或重搏波波谷点和波峰位置,图中8(a)、9(a)均为使用本文方法识别时,各特征点在微分信号中的位置.
从图中可看出,2种状态下对于一些特征点不明显的情况,文献[5]方法容易误检或漏检,文献[6]方法识别的特征点间距过大,部分特征没有极值点或多极值点干扰的情况下不能够准确识别,不利于后续评估血管疾病,而TDDR法在两种状态下,均能准确识别特征点,适用性更强.本文以人为标记的各特征点位置为标准,使用不同方法识别测试者在静息状态下(50组,平均每组36个脉搏周期,共1 800个)和运动状态下(50组,平均每组45个脉搏周期,共2 250个)脉搏波的各特征点.由于部分变异的脉搏波特征点难以精确到起始点,本文用微分信号中极值点的均值代替,考虑到标记点与特征点识别的位置存在一定误差,因此在采集频率为1 kHz,允许10 ms的误差范围内,统计脉搏波特征点的准确率,如表2~3所示.可见,使用本文提出的TDDR识别方法,对起点和波峰点识别准确率都达到100%,静息状态下潮波d、e准确率分别为98.28%和97.25%,重搏波f、g准确率分别达到98.14%和99.19%;而运动状态下潮波d、e点准确率为94.23%和90.77%,重搏波f、g点准确率为91.93%和95.38%,均优于传统方法.
表 2. 静息状态下特征点定位准确率(%)
Table 2. Accuracy of feature point positioning in resting state (%)
|
表 3. 运动状态下特征点定位准确率(%)
Table 3. Accuracy of feature point positioning under motion (%)
|
5 结论
本文采用PDMS封装后的FBG柔性传感器对脉搏波信号进行采集,采用EMD自适应分解的方法对采集的信号进行预处理,根据不同状态下脉搏波的特征点在时域微分信号中的相对位置关系,针对脉搏波信号最可能出现的四种情况,提出了一种定位各特征点的TDDR方法.实验结果表明,该方法选择在逐渐缩小的范围内定位识别,减少了不必要的干扰,能够全部准确识别起点与波峰的特征点,在静息状态下,潮波d、e点的识别准确率为98.28%和97.25%,重搏波f、g点的识别准确率为98.14%和99.19%;在运动状态下,潮波d、e的识别准确率分别为94.23%和90.77%,重搏波f、g识别准确率分别为91.93%和95.38%;解决了不同类型脉搏波的特征定位方法,具有识别准确率高,抗干扰能力强等特点.通过特征点的准确识别,可为后续的脉搏速率、周期、反射波和舒张期增强指数等生理信息判别提供依据.由于本文选取的运动状态为剧烈运动,没有讨论不同程度运动的特征点识别情况,因此后续将分别研究讨论,以提高其普遍适用性.
[1] 郭维, 刘光达, 焦阳. 基于脉搏波信号和血管弹性腔模型的动脉血压连续测量方法[J]. 医用生物力学, 2012, 27(1): 84-89.
GUO Wei, LIU Guang-da, JIAO Yang. Continuous measurement of arterial blood pressure based on pulse wave signal and vessel elastic chamber model[J]. Journal of Medical Biomechanics, 2012, 27(1): 84-89.
[2] KURASAWA S, KOYAMA S, ISHIZAWA H. Verification of non-invasive blood glucose measurement method based on pulse wave signal detected by FBG sensor system[J]. Sensors, 2017, 17(12): 2702.
[3] 张永会, 高长青, 王嵘. 脉搏波分析方法及其应用[J]. 北京生物医学工程, 2019, 38(3): 319-326.
ZHANG Yong-hui, GAO Chang-qing, WANG Rong. Methods of pulse wave analysis and its application[J]. Beijing Biomedical Engineering, 2019, 38(3): 319-326.
[4] 朱耀斌, 李志强, 丁楠. 脉搏传感器应用的研究进展[J]. 中华实用诊断与治疗杂志, 2019, 33(3): 306-309.
ZHU Yao-bin, LI Zhi-qiang, DING Nan. Research progress of pulse sensor[J]. Journal of Chinese Practical Diagnosis and Therapy, 2019, 33(3): 306-309.
[5] LUKASZ D, MARIUSZ K, FRANCISZEK W S. Fiber Bragg grating strain sensor incorporated to monitor patient vital signs during MRI[J]. IEEE Sensors Journal, 2013, 13(12): 4986-4991.
[6] CHEN Z. Intensity-modulated microbend fiber optic sensor for respiratory monitoring and gating during MRI[J]. IEEE Transactions on Biomedical Engineering, 2013, 60(9): 2655-2662.
[7] JOAO P C, JOSE H C, RUI P R. Application of fiber Bragg gratings to wearable garments[J]. IEEE Sensors Journal, 2012, 12(1/2): 261-266.
[8] 孙薇, 唐宁, 江贵平. 脉搏波信号特征点识别与预处理方法研究[J]. 生物医学工程学杂志, 2015, 32(1): 197-201.
SUN Wei, TANG Ning, JIANG Gui-ping. Study of characteristic point identification and preprocessing method for pulse wave signals[J]. Journal of Biomedical Engineering, 2015, 32(1): 197-201.
[9] 季忠, 刘旭. 基于波形特征和小波的脉搏波特征点识别研究[J]. 仪器仪表学报, 2016, 37(2): 379-386.
JI Zhong, LIU Xu. Study on feature points recognition of pulse wave based on waveform feature and wavelet[J]. Chinese Journal of Scientific Instrument, 2016, 37(2): 379-386.
[10] 刘铁根, 王双, 江俊峰. 航空航天光纤传感技术研究进展[J]. 仪器仪表学报, 2014, 35(8): 1681-1692.
LIU Tie-gen, WANG Shuang, JIANG Jun-feng. Advances in optical fiber sensing technology for aviation and aerospace application[J]. Chinese Journal of Scientific Instrument, 2014, 35(8): 1681-1692.
[11] 王彦, 秦楠, 刘吉虹. 基于光纤光栅的温度与压力柔性传感性能测试[J]. 仪器仪表学报, 2019, 40(3): 93-98.
WANG Yan, QIN Nan, LIU Ji-hong. Test of temperature and pressure flexible sensor based on optical fiber Bragg grating[J]. Chinese Journal of Scientific Instrument, 2019, 40(3): 93-98.
[12] HLENSCHI C, CORODEANU S, CHIRIAC H. Magnetoelastic sensors for the detections of pulse waves[J]. IEEE Transactions on Magnetics, 2013(1): 117-119.
[13] 崔冰波, 陈熙源, 宋锐. EMD阈值滤波在光纤陀螺漂移信号去噪中的应用[J]. 光学学报, 2015, 35(2): 53-58.
CUI Bing-bo, CHEN Xi-yuan, SONG Rui. Application of EMD threshold filtering for fiber optical gyro drift signal de-noising[J]. Acta Optica Sinica, 2015, 35(2): 53-58.
[14] 陈真诚, 吴贤亮, 赵飞骏. EEMD结合小波阈值的光电容积脉搏波信号降噪[J]. 光学精密工程, 2019, 27(6): 1327-1334.
[16] 刘文彦, 王璐, 姚阳. 脉搏波传导速度与反射波增强指数相关性分析[J]. 中国医疗设备, 2018, 33(8): 21-24+29.
LIU Wen-yan, WANG Lu, YAO Yang. Correlation analysis of pulse wave velocity and augmentation index[J]. China Medical Devices, 2018, 33(8): 21-24+29.
[17] 张金玲, 崔彤, 刘为斌. 基于自适应时间窗函数优化的心电特征波形识别[J]. 北京邮电大学学报, 2019, 42(4): 82-88.
ZHANG Jin-ling, CUI Tong, LIU Wei-bin. adaptive time window function optimization based electrocardiography feature waveform recognition[J]. Journal of Beijing University of Posts and Telecommunications, 2019, 42(4): 82-88.
[18] JOSEPH E, PETER U. Pulse wave velocities derived from cuff ambulatory pulse wave analysis effects of age and systolic blood pressure[J]. Hypertension: An Official Journal of the American Heart Association, 2019, 74(1): 111-116.
Article Outline
范保存, 王彦, 黄晨晨, 葛子阳, 金萍. 基于时域微分周期比的脉搏波信号特征识别[J]. 光子学报, 2020, 49(12): 51. Bao-cun FAN, Yan WANG, Chen-chen HUANG, Zi-yang GE, Ping JIN. Pulse Wave Signal Feature Recognition Based on Time-domain Differential Period Ratio[J]. ACTA PHOTONICA SINICA, 2020, 49(12): 51.