γ 射线辐照及粒径对芦苇秸秆酶解发酵的影响
随着工业化及社会经济的快速发展,能源安全和环境污染问题日益成为世界可持续发展的主要制约因素,随着化石能源的逐渐枯竭,发展绿色可再生能源刻不容缓。生物燃料乙醇因其可再生、环境友好、促进农业发展等优势,成为替代汽油消费的潜在选择。富含木质纤维素的农林废弃物因其量大、经济、且不与人和动物争粮等特点,已成为第二代生物燃料乙醇的主要原料。研究表明:富含木质纤维素的农林废弃物因其量大、经济、且不与人和动物争粮等特点,已成为第二代生物燃料乙醇的主要生产原料。研究表明,芦苇(Phragmites australias)的木质纤维素含量,特别是纤维素含量明显高于常见农林废弃物(如稻草、油菜秸秆、玉米秸秆等),而纤维素是生物燃料乙醇的主要糖源[1-2]。因此,以芦苇为原料发酵产乙醇成为研究热点[3-4]。
利用生物质生产燃料乙醇的工艺流程为:原料预处理—水解糖化—发酵—纯化—精馏[5]。纤维素是生物质制备燃料乙醇的主要原材料,其被高度聚合的木质素包裹,难以与生物催化剂接触,严重降低反应效率。因此,在水解糖化之前,预处理破坏木质素结构、膨化纤维素成分是不可或缺的步骤。传统的预处理方式有物理方法(机械挤压、微波、爆破等)、化学方法(稀酸处理、碱处理等)、生物方法(真菌生物预处理等)、离子液体法等。诸多研究表明:相对于常用的预处理方式,如粉碎、蒸汽爆破、酸碱处理及生物方法等[6-9],高能辐照技术具有操作简单、破坏程度大、酶解转化率提升明显、反应条件温和、对环境友好等优势,目前已成为生物质高效利用过程中的有效物理预处理手段[10]。
高能辐照处理对生物质材料的粒径也有一定的影响,在一定的吸收剂量范围内,小粒径的比重会随着吸收剂量而增大。Wu等[11]研究发现,稻草、油菜秸秆、玉米秸秆经相同粉碎时间的粉碎处理后,其粒径r˂0.075 mm的颗粒均随着吸收剂量的增加而显著增加,其中,未经辐照处理和经1 000 kGy吸收剂量处理后的样品,其粒径r˂0.075 mm的颗粒的比率分别为3.64%~9.83%和36.70%~54.64%。唐洪涛等[12]研究发现,玉米秸秆经800 kGy辐照处理后,秸秆粒度r˂0.075 mm的颗粒占比由7.6%(未辐照)增加至42.4%。研究表明,生物质经机械粉碎至不同颗粒尺度,显著影响其酶解后葡萄糖产量。Ji等[13]以稻草为研究对象,研究发现,稻草粉碎至细胞尺度(˂0.050⁓0.030 mm)后,其结晶度显著降低,酶解后葡萄糖产量为287.07 mg/g,较组织尺度(0.500⁓0.100 mm)颗粒样品提高149.02%。目前,关于粒径对生物质酶解发酵影响的相关研究多将生物质颗粒进行多级过筛,对于单级过筛的样品的酶解发酵研究较少,而多级过筛操作因其成本高、难度大严重制约工业化利用。以生物质为原料的绿色制造研究是目前的研究热点,原料的粒径选取多为细粉碎范畴(0.500⁓0.100 mm)[14-15],但关于最适粒径范围,特别是结合辐照处理的最适粒径范围研究甚少。本试验以芦苇为研究对象,通过辐照结合机械粉碎预处理,经过不同孔径的单一筛筛分,对比粒径分布、粉碎能耗、组分含量及纤维素酶解转化率、纤维素乙醇转化率等,确定最佳过筛粒径,满足工业化需求,以期为生物质大规模利用提供理论依据和技术支撑。
1 材料与方法
1.1 材料与试剂
芦苇秸秆:2018年11月采集于湖南省洞庭湖区。酿酒酵母(Saccharomyces cerevisiae):中国工业微生物菌种保藏管理中心(China center of industrial culture collection,CICC),编号:33068。甲酸、乙酸、无水葡萄糖、木糖、阿拉伯糖、纤维二糖、无水乙醇、硫酸铵、磷酸二氢钾、无水硫酸镁、硫酸、磷酸氢二铵、无水氯化钙、氢氧化钙、氢氧化钠(均为分析纯):国药集团化学试剂有限公司;酵母粉(生化试剂):广东环凯微生物科技有限公司;纤维素酶(滤纸酶活100 FPU/mL):Novozymes公司。发酵培养基:硫酸铵2 g/L、磷酸二氢钾5 g/L、无水硫酸镁1 g/L、无水氯化钙0.2 g/L、酵母粉5 g/L;pH≈6(碳源为玉米秸秆),115 ℃灭菌20 min。活化培养基:葡萄糖50 g/L、硫酸铵2 g/L、磷酸二氢钾5 g/L、无水硫酸镁1 g/L、无水氯化钙0.2 g/L、酵母粉5 g/L;pH≈6,115 ℃灭菌20 min。
1.2 仪器与设备
60Co γ辐照装置(源强2.96×1016 Bq):湖南省核农学与航天育种研究所;Thermo Ultimate 3000高效液相色谱仪(High performance liquid chromatography,HPLC):赛默飞世尔科技(中国)有限公司;TG16-Ⅱ台式高速离心机:长沙平凡仪器仪表有限公司;YXQ-LS-50S11压力蒸汽灭菌器:上海博迅实业有限公司医疗设备厂;HZQ-F100恒温摇床:常州诺基仪器有限公司;BlueStar A 紫外分光光度计:北京莱伯泰科仪器股份有限公司;中草药粉碎机(FW177):天津市泰斯特仪器有限公司;落地式洁净工作台(SW-CJ-2D):邦西仪器科技(上海)有限公司;电子天平(BSA224S):赛多利斯科学仪器(北京)有限公司;电热恒温干燥箱(BGZ-76):上海博迅实业有限公司。
1.3 方法
1.3.1 芦苇秸秆辐照处理
芦苇秸秆自然晒干,切成10⁓15 cm的小段,装入金属样品盒,于室温条件下用60Co γ射线进行辐照预处理,剂量率为1.25 kGy/h,吸收剂量分别为0 kGy、200 kGy、300 kGy、400 kGy、500 kGy(实际吸收剂量分别为0 kGy、206 kGy、312 kGy、404 kGy、498 kGy),处理后备用。
1.3.2 芦苇秸秆粉碎处理
称取§1.3.1所得的试验材料1 kg(5份),采用中草药粉碎机(24 000 r/min,P=2 kW/h)粉碎处理30 s,其中4份,每份分别过孔径0.850 mm、0.425 mm、0.250 mm、0.180 mm筛,收集粒径r˂0.850 mm、r˂0.425 mm、r˂0.250 mm、r˂0.180 mm的样品;第五份不过筛,收取所有颗粒(All)并分别称重,自封袋保存,备用。
粉碎能耗(kWh)=(芦苇杆原料质量/m)×粉碎时间×仪器功率。其中:m为获得相应粒径范围的芦苇杆的质量。
1.3.3 水提处理
(1)水提。称取§1.3.2所述粒径的吸收剂量分别为0 kGy、206 kGy、404 kGy的芦苇秸秆3 g(精确至0.000 1 g),置于具塞三角瓶中,按1∶30的比例加入去离子水,于50 ℃ 200 r/min条件下浸提处理2 h后过滤,滤渣烘干至恒重,滤液测定葡萄糖和木糖含量,滤液备用;
(2)水提液酸水解。量取§1.3.3(1)滤液14 mL,加入0.5 mL 72%硫酸,置于高压灭菌锅中,121 ℃条件下反应1 h后取出,6 000 r/min离心5 min,取上清测定葡萄糖和木糖含量,计算样品中可溶性葡聚糖、木聚糖的含量,见公式(
1.3.4 组分含量测定
称取烘干的试验样品0.3 g(精确至0.000 1 g),加入3 mL 72%硫酸,30 ℃条件下水浴反应1 h,每5⁓10 min振摇1次,加入蒸馏水84 mL,置于高压灭菌锅中,121 ℃条件下反应1 h后取出,滤纸过滤,滤液、滤渣备用。
(1)葡聚糖和木聚糖含量的测定。滤液采用HPLC测定葡萄糖和木糖含量,计算样品中葡聚糖、木聚糖的含量,计算见公式(
(2)木质素含量的测定:滤液采用分光光度计在320 nm波长下测定吸光度,按以下公式计算酸溶性木质素含量;滤渣105 ℃烘干至恒重,称重,即为酸不溶性木质素质量;酸溶性木质素与酸不溶性木质素含量总和即为木质素含量,见公式(
式中:ε=30 L/(g·cm)
1.3.5 酶解
称取不同粒径吸收剂量分别为0 kGy、206 kGy、404 kGy辐照的芦苇秸秆2.0 g(精确至0.000 1 g),按固液比1∶15加入0.1 mol/L的乙酸-乙酸钠缓冲溶液(pH=4.8),纤维素酶加入量20 FPU/g,摇匀后置于50 ℃ 130 r/min条件下进行酶解反应。反应48 h后取样0.5 mL,6 000 r/min 离心5 min后取上清200 μL,加流动相溶液稀释5倍,过膜,备用。通过测定葡萄糖含量,计算出葡聚糖转化率,见
1.3.6 分步糖化发酵
采用发酵培养基替代§1.3.5乙酸-乙酸钠缓冲溶液,按照§1.3.5试验步骤进行酶解处理72 h后,6 000 r/min离心5 min后取上清10~50 mL,发酵专用具塞锥形瓶,115 ℃高压灭菌20 min,取出放置室温,接入1 mL种子培养液,置于恒温摇床中,37 ℃、150 r/min条件下进行发酵,发酵24 h后,取样0.5 mL,6 000 r/min离心5 min后取上清200 μL,加流动相溶液稀释5倍,过膜,备用。通过测定乙醇含量,计算出乙醇转化率,见
式中:理论乙醇转化质量=样品纤维素质量×1.1×0.51。
1.4 测定方法
1.4.1 还原糖含量测定
利用HPLC测定还原糖含量。色谱柱:Bio-RAD AminexR HPX-87H Ion Exclusion Column(300 mm×7.8 mm);流动相:0.005 mol/L H2SO4;流速:0.6 mL/min;柱温:55 ℃;柱后冷却温度:30 ℃;检测器:示差折光检测器(Refractive indexdetector,RID);检测器温度:45 ℃;进样体积:10 μL。
1.4.2 乙醇含量测定
利用HPLC测定乙醇含量,具体操作同HPLC 测定还原糖含量。
1.5 数据处理
采用SAS 8.1和Microsoft Excel 2010分析整理数据;Origin 8.0制图。
2 结果与讨论
2.1 辐照处理对芦苇秸秆粒径分布及粉碎能耗的影响
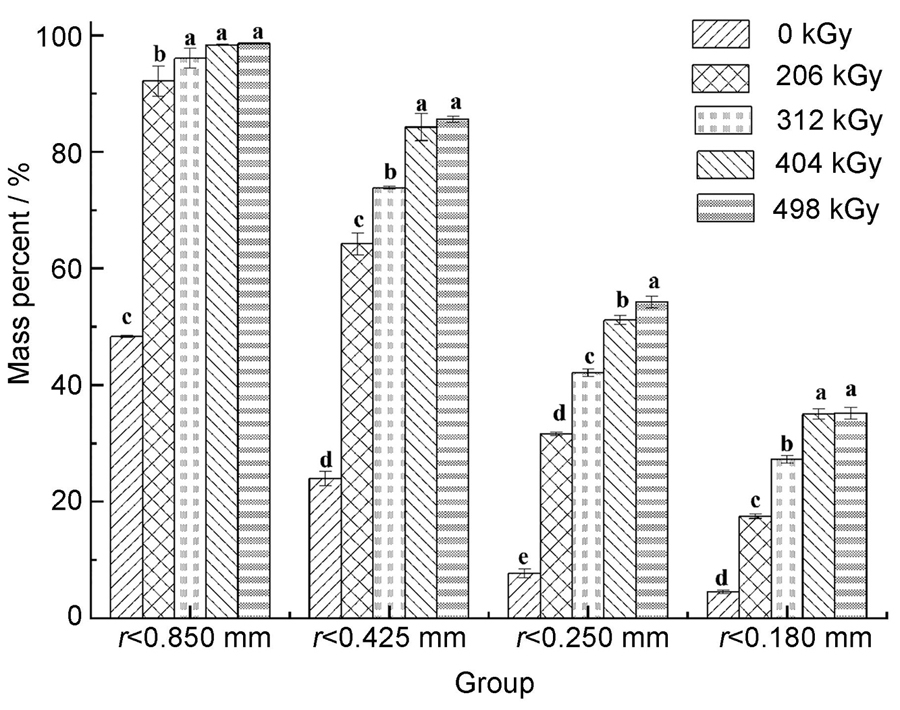
图 1. 不同吸收剂量下芦苇秸秆粉碎粒径分布图;a、b、c、d,同一指标不同字母表示存在显著差异(p<0.05)
Fig. 1. Particle size distribution of crushed reed straws at different absorbed irradiation doses; a, b, c, d, there are significant differences in the same series with different letters (p<0.05)
由

图 2. 不同剂量辐照处理后芦苇秸秆粉碎至不同粒径范围的粉碎能耗;a、b、c、d,同一指标不同字母表示存在显著差异(p<0.05)
Fig. 2. Comminution energy of reed straws to different particle size ranges under different absorbed doses; a, b, c, d, there are significant differences in the same series with different letters (p<0.05)
2.2 辐照及粉碎处理对芦苇组分含量的影响
表 1. 辐照处理芦苇秸秆在不同粒径下的水提液成分及组分测定
Table 1. Determination of components and components of water extract of irradiated reed straws under different particle sizes
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
对于芦苇秸秆的木质纤维素含量,随着吸收剂量的增加,纤维素和半纤维素的含量在同一粒径范围均有显著下降,木质素含量的变化不明显。吸收剂量为206 kGy和404 kGy的芦苇秸秆,其未过筛、粒径为r˂0.850 mm、r˂0.425 mm、r˂0.250 mm、r˂0.180 mm的样品的纤维素含量较未辐照处理芦苇秸秆相应粒径样品分别降低3.62%、2.24%、0.38%、1.63%、1.15%和5.91%、4.91%、2.42%、4.27%、4.15%;半纤维素含量分别降低3.79%、4.08%、4.25%、5.11%、4.46%和3.79%、6.48%、6.82%、7.20%、6.86%。原因是随着吸收剂量的增加,辐照处理对芦苇秸秆样品的木质纤维素结构破坏逐渐增强,其中的部分纤维素、半纤维素被降解成小分子聚糖,或进一步降解生成小分子单糖或多糖等[20]。对于吸收剂量相同的芦苇秸秆样品,随着粒径的减小,其纤维素含量也有显著变化,未辐照、吸收剂量为206 kGy、404 kGy的芦苇秸秆样品,其粒径r˂0.180 mm的芦苇秸秆样品的纤维素含量较粒径r˂0.850 mm的样品分别减小6.26%、5.21%、5.52%,原因是,随着样品粒径的减小,在水洗过程中与水的接触面积增加,溶出的可溶物增加,因此水洗滤渣中木质纤维素含量降低。
2.3 辐照及样品粒径对芦苇秸秆葡聚糖酶解转化率的影响
由

图 3. 不同吸收剂量下芦苇秸秆的不同粒径样品的纤维素酶解转化率;a、b、c、d,同一指标不同字母表示存在显著差异(p<0.05)
Fig. 3. Cellulose enzymatic hydrolysis conversion rate of reed straws with different particle sizes under different absorbed doses; a, b, c, d, there are significant differences in the same series with different letters (p<0.05)
不同吸收剂量及粒径的芦苇秸秆的纤维素酶解转化率方差分析如
表 2. 不同吸收剂量及粒径的芦苇秸秆的纤维素酶解转化率方差分析
Table 2. Variance analysis of cellulose enzymatic hydrolysis conversion of reed straws with different absorbed doses and particle size
|
2.4 辐照及样品粒径对芦苇秸秆纤维素乙醇转化率的影响
由

图 4. 不同吸收剂量下芦苇秸秆的不同粒径样品的纤维素乙醇转化率;a、b、c、d,同一指标不同字母表示存在显著差异(p<0.05)
Fig. 4. The cellulose ethanol conversion rates of reed straws with different particle sizes treated with different absorbed doses; a, b, c, d, there are significant differences in the same series with different letters (p<0.05)
不同吸收剂量及粒径的芦苇秸秆的纤维素乙醇转化率方差分析如
表 3. 不同吸收剂量及粒径的芦苇秸秆纤维素乙醇转化率方差分析
Table 3. Variance analysis of cellulose ethanol conversion of reed straws with different absorbed doses and particle size
|
2.5 过筛孔径对芦苇秸秆样品粉碎能耗、葡聚糖转化率、乙醇转化率的影响
表 4. 过不同粒径筛的芦苇秸秆样品粉碎能耗、纤维素酶解转化率、纤维素乙醇转化率的增加比率
Table 4. Increased ratios of comminution energy, cellulose enzymatic hydrolysis conversion rates and cellulose ethanol conversion rates of reed straws passing through sieves with different particle sizes
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3 结论
辐照能破坏芦苇木质纤维素结构,纤维素、半纤维素发生降解生成水溶性组分;粉碎过筛处理能在一定程度上提高芦苇秸秆后续的酶解糖化和发酵产乙醇效率,且吸收剂量、粒径大小以及两者之间的交互作用均对芦苇秸秆纤维素酶解转化率和乙醇转化率有显著影响。试验研究结果显示:未辐照芦苇秸秆样品的最佳过筛孔径为0.850 mm,获得r<0.850 mm的芦苇秸秆样品的纤维素酶解转化率为8.503%,纤维素乙醇转化率为6.207%;吸收剂量为206 kGy和404 kGy的芦苇秸秆样品,其最佳过筛孔径为0.425 mm,所获得r<0.850 mm的芦苇秸秆样品的纤维素酶解转化率分别为10.437%和14.260%,纤维素乙醇转化率分别为9.768%和8.833%;而芦苇秸秆样品纤维素乙醇转化率随着吸收剂量进一步增加而减少的原因需要进一步研究。
[1] Zhu S D, Wu Y X, Yu Z N, et al. Pretreatment by microwave/alkali of rice straw and its enzymic hydrolysis[J]. Process Biochemistry, 2005, 40(9): 3082-3086.
[2] Jin A X, Ren J L, Peng F, et al. Comparative characterization of degraded and non-degradative hemicelluloses from barley straw and maize stems: composition, structure, and thermal properties[J]. Carbohydrate Polymers, 2009, 78(3): 609-619.
[3] 詹怀宇, 付时雨, 李海龙. 我国非木材纤维制浆的发展概况与技术进步(之二) 蔗渣、芦苇和棉秆[J]. 中华纸业, 2011, 32(10): 6-9.
ZHAN Huaiyu, FU Shiyu, LI Hailong. The development overview and technical progress for non-wood fiber pulping of bagasse, reed and cotton stalk[J]. China Pulp&Paper Industry, 2011, 32(10): 6-9.
[4] Zhang C Y, Su X J, Xiong X Y, et al. 60 Co-γ radiation-induced changes in the physical and chemical properties of rapeseed straw[J]. Biomass and Bioenergy, 2016, 85: 207-214.
[5] 张爱萍, 谢君. 生物质制乙醇预处理方法的研究进展[J]. 华南农业大学学报, 2014, 35(4): 77-84.
ZHANG Aiping, XIE Jun. Pretreatment method for production of bioethanol with lignocellulosic material[J]. Journal of South China Agricultural University, 2014, 35(4): 77-84.
[6] 赵晓燕, 朱海涛, 张桂香, 等. 超微粉碎预处理对玉米秸杆酶解液中还原糖组分的影响[J]. 粮油食品科技, 2015, 23(6): 96-98.
ZHAO Xiaoyan, ZHU Haitao, ZHANG Guixiang, et al. Effect of superfine comminution on reducing sugar components in corn stalk enzymatic hydrolysate[J]. Science and Technology of Cereals, Oils and Foods, 2015, 23(6): 96-98.
[7] Jiang S T, Guo N. The steam explosion pretreatment and enzymatic hydrolysis of wheat bran[J]. Energy Sources, Part A: Recovery, Utilization and Environmental Effects, 2016, 38(2): 295-299.
[8] Sindhu R, Kuttiraja M, Binod P, et al. Physicochemical characterization of alkali pretreated sugarcane tops and optimization of enzymatic saccharification using response surface methodology[J]. Renewable Energy, 2014, 62: 362-368.
[9] 甄静, 李冠杰, 李伟, 等. 毛栓孔菌XYG422菌株产漆酶发酵条件优化及对玉米秸秆生物降解的研究[J]. 菌物学报, 2017, 36(6): 718-729.
ZHEN Jing, LI Guanjie, LI Wei, et al. Fermentation condition optimization of laccase producing strain Trametes hirsuta XYG422 and its activity on corn straw degradation[J]. Mycosystema, 2017, 36(6): 718-729.
[10] 张春艳, 谭兴和, 熊兴耀, 等. 油菜秸秆60Co-γ辐照降解产物分析[J]. 湖南农业大学学报(自然科学版), 2017, 43(1): 92-97.
ZHANG Chunyan, TAN Xinghe, XIONG Xingyao, et al. Analysis of degradation products of rapeseed straw irradiated with 60Co-γ[J]. Journal of Hunan Agricultural University (Natural Sciences), 2017, 43(1): 92-97.
[11] Wu X F, Chen L, He W Q, et al. Characterize the physicochemical structure and enzymatic efficiency of agricultural residues exposed to γ-irradiation pretreatment[J]. Industrial Crops and Products, 2020, 150: 112228.
[12] 唐洪涛, 哈益明, 王锋. γ射线辐照玉米秸秆预处理对酶解产糖的影响[J]. 辐射研究与辐射工艺学报, 2011, 29(5): 307-313.
TANG Hongtao, Yiming HA, WANG Feng. Effect of γ-rays radiation pretreatment on enzymatic hydrolysis of corn straw for producing sugar[J]. Journal of Radiation Research and Radiation Processing, 2011, 29(5): 307-313.
[13] Ji G Y, Han L J, Gao C F, et al. Quantitative approaches for illustrating correlations among the mechanical fragmentation scales, crystallinity and enzymatic hydrolysis glucose yield of rice straw[J]. Bioresource Technology, 2017, 241: 262-268.
[14] Barakat A, Mayer-Laigle C, Solhy A, et al. Mechanical pretreatments of lignocellulosic biomass: towards facile and environmentally sound technologies for biofuels production[J]. RSC Advances, 2014, 4(89): 48109-48127.
[15] 余燕燕, 李以琳, 楼雨寒, 等. 低共熔溶剂解离木纤维时木质素缩合对纤维素酶解的影响[J]. 林业工程学报, 2021, 6(6): 101-108.
YU Yanyan, LI Yilin, LOU Yuhan, et al. Effect of lignin condensation on cellulose enzymatic hydrolysis during deep eutectic solvent fractionation of lignocellulose[J]. Journal of Forestry Engineering, 2021, 6(6): 101-108.
[16] Liu Y, Guo L J, Wang L Y, et al. Irradiation pretreatment facilitates the achievement of high total sugars concentration from lignocellulose biomass[J]. Bioresource Technology, 2017, 232: 270-277.
[17] Liu Y, Zhou H, Wang L Y, et al. Improving Saccharomyces cerevisiae growth against lignocellulose-derived inhibitors as well as maximizing ethanol production by a combination proposal of γ-irradiation pretreatment with in situ detoxification[J]. Chemical Engineering Journal, 2016, 287: 302-312.
[18] 郭栋豪, 陈亮, 武小芬, 等. 辐照与粉碎对玉米秸秆酶解葡聚糖转化率的影响[J]. 河南农业科学, 2018, 47(1): 139-144.
GUO Donghao, CHEN Liang, WU Xiaofen, et al. Effects of irradiation and smash on the glucan conversion rate by enzymatic hydrolysis of corn stalk[J]. Journal of Henan Agricultural Sciences, 2018, 47(1): 139-144.
[19] 武小芬, 陈亮, 齐慧, 等. 钴-60伽马射线辐照对甲酸分离玉米芯成分的影响[J]. 辐射研究与辐射工艺学报, 2018, 36(1): 010402.
WU Xiaofen, CHEN Liang, QI Hui, et al. Effect of cobalt-60 gamma-ray irradiation on separation of components from corncob by formic acid[J]. Journal of Radiation Research and Radiation Processing, 2018, 36(1): 010402.
[20] Zhu L, Yu B, Chen H, et al. Comparisons of the micronization, steam explosion, and gamma irradiation treatment on chemical composition, structure, physico-chemical properties, and in vitro digestibility of dietary fiber from soybean hulls[J]. Food Chemistry, 2022, 366: 130618.
[21] 张勇, 郭栋豪, 王克勤, 等. γ射线辐照预处理玉米秸秆发酵产乙醇的研究[J]. 中国酿造, 2018, 37(9): 58-61.
ZHANG Yong, GUO Donghao, WANG Keqin, et al. Fermentation for ethanol production with γ ray irradiation-pretreated corn straw[J]. China Brewing, 2018, 37(9): 58-61.
[22] Islam S M M, Elliott J R, Ju L K. Minimization of fermentation inhibitor generation by carbon dioxide-water based pretreatment and enzyme hydrolysis of guayule biomass[J]. Bioresource Technology, 2018, 251: 84-92.
Article Outline
齐慧, 陈亮, 武小芬, 刘安, 王丹阳, 张勇, 邓明, 王克勤.



