水果糖度可见-近红外光谱手持式检测装置开发与试验
1 引言
可见-近红外光谱分析为代表的无损检测技术在水果糖度的快速、 无损检测方面得到了广泛应用[1]。 水果糖度的便携式或手持式装置, 可以实现水果糖度的快速、 现场检测, 满足水果样品抽检、 定级以至田间管理[2]。 目前, 如久保田株式会社, FELIX以及Atago等都推出了相关产品。 但上述国外公司的产品价格较高, 检测样品单一, 不易于后期模型和设备的维护, 使用成本较高。
在近几年的研究中, 国内外研究人员借助小型商品化光谱仪器, 也开发了具有类似功能的样机。 样机的开发主要集中在用于水果光谱采集探头的设计以及后续对光谱仪的控制。 Yang[3]、 Guo[4]等开发了用于猕猴桃、 油桃糖度检测的便携式装置, 王凡[5]、 郭志明[6]等设计了用于番茄糖度、 番茄红素等指标分析的检测装置。 除了利用商品化光谱仪外, Yu等[7]利用线性渐变滤光片自行开发了用于梨果糖度检测的便携式装置。 赵娟等[8]基于所选10个特征波长的LED和硅光电二极管, 开发了用于苹果糖度检测的便携式装置, 虽然成本有所降低, 但精度有所下降。 借助便携式光谱仪可以直接用于树上柑橘[9]等水果品质的无损分析, 但大都没有形成最终检测装置。 分析发现, 上述装置成本较高, 大都针对同种水果进行评价, 且均针对开发的一台装置进行检验, 缺少模型在不同装置间的传递等方面的探讨。
在前期研究中, 本课题组以海洋光学USB2000+光谱仪和嵌入式操作系统为核心, 成功研制了用于多种水果糖度检测的背带式检测装置[10]。 虽然取得了较好的检测结果, 但成本高, 携带不便。 本研究继续以微型光谱仪为核心, 开发了成本更低, 更轻便的手持式水果糖度检测装置, 并在实验室和果园环境对装置的检测精度进行检验, 同时探讨了糖度模型在不同装置间的传递。
1 实验部分
1.1 硬件系统设计
水果糖度手持式可见-近红外光谱检测装置硬件系统主要包括微型光谱仪、 卤素灯、 单片机及外围电路、 锂电池、 OLED显示屏等部分。 为了减小手持式装置的体积、 节约成本, 该装置不具备存储光谱数据的功能, 因此在采集光谱数据时需要将装置与计算机通过串口相连。 待模型构建并导入单片机后, 方可单独使用。
光谱仪为微型光谱仪(C11708MA, 滨松, 日本), 波长范围为640~1 050 nm, 该光谱仪体积小, 重量轻。 采用小型卤素灯, 功率1.5 W。 检测时采用漫透射方式[5], 将水果放置于探头之上, 赤道部位紧贴中间接收孔, 卤素灯发出的光, 经过与水果作用后, 被距卤素灯16 mm接收孔下方的微型光谱仪接收。
单片机选用STM32单片机, 自行设计光谱仪驱动电路。 实现光谱按设定积分时间进行获取。 为增加光谱稳定性, 获取3次水果光谱的平均值作为最终光谱。 串口用于和上位机软件通讯。 OLED显示屏用于显示水果糖度预测值。 电源容量6 000 mah锂电池, 工作时间约为2.5~3 h。 在采集可见-近红外光谱时常常进行白参考校正。 本研究针对开发的装置结构, 设计了如图1所示的白参考校正模块。 另外, 该装置配有遮光罩用于室外水果的光谱采集, 减少阳光等杂散光对光谱采集影响。 图1为开发的手持式水果糖度可见-近红外光谱检测装置实物图以及配套的上位机光谱采集界面。
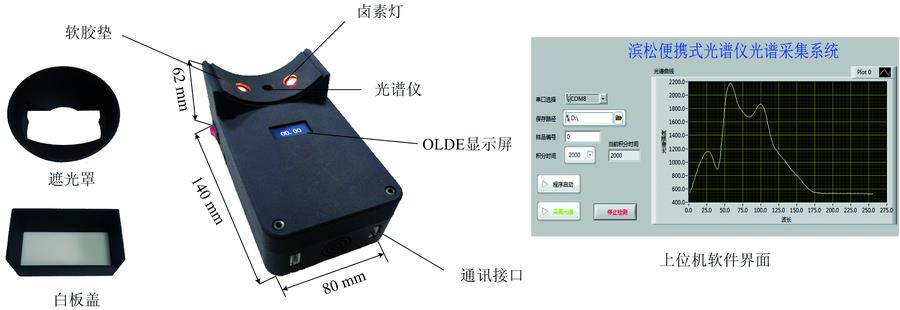
图 1. 水果糖度手持式检测装置图
Fig. 1. Image of the developed handheld visible/near infrared device for detecting fruit sugar content
1.2 软件系统设计
检测装置的软件系统基于Keil 5平台开发, 采用C语言进行程序编写。 实现水果漫透射可见-近红外光谱信息的采集、 数据传输、 结果显示等功能。 上位机配套LabView编写的光谱采集软件, 通过串口和手持式检测装置通讯, 通过上位机设定手持式装置的积分时间, 完成水果光谱信息在指定积分时间下的获取。
1.3 材料及水果光谱采集
以大桃、 苹果作为实验对象。 样机共开发两台, 分别编号为P-NIR-01和P-NIR-02。 2020年8月份在北京平谷大桃果园进行实验。 借助笔记本电脑, 完成树上水果光谱信息采集, 采集前获取白参考光谱, 随后将遮光罩套在探头上方用于树上水果光谱采集。 采集水果光谱后对样品进行编号, 共采摘大桃150个, 积分时间设置为900 ms。 田间光谱信息采集只利用了P-NIR-01装置。 采集完成后, 运回实验室。 从中随机选取110个大桃作为校正集, 剩余样本作为预测集。 实验室环境下的光谱采集, 同时采用上述2台装置获取大桃光谱信息, 积分时间都设置为900 ms。
采取同样方法, 采用编号为P-NIR-01装置于2020年10月在北京昌平苹果园获取树上苹果光谱信息, 积分时间为600 ms, 共采集富士苹果140个。 从中随机选取100个苹果作为校正集。 运回实验室后采用2台装置进行光谱信息采集, 采集参数同样设置为600 ms。
在实验室采集条件下, 研究了模型在上述2台装置间的传递。 选择P-NIR-01作为主机(也称作源机), P-NIR-02作为从机(也称作目标机)。 从校正集光谱中选取一定数量样本作为标准样品, 用于确定主机光谱与从机光谱的对应关系。 主机对应的校正集用于模型构建, 主机的预测集用于对模型的检测精度进行评价, 从机的预测集用于模型传递的评价。
1.4 水果糖度实测值获取
光谱采集完成后, 从光谱采集的赤道部位切取厚度为10 mm左右带果皮果肉, 经纱布过滤挤汁后, 滴到折光仪(PAL-1, ATAGO, 日本)镜面, 读数并记录。 结果如表1所示。
表 1. 水果糖度实测值
Table 1. Statistics of fruit sugar content measurement
|
1.5 光谱数据处理
由于采集的光谱信息在波段首尾两端均存在较大噪声, 因此选择600~950 nm范围进行后续分析。 首先参照式(1)对原始光谱数据进行白校正得到透射率光谱(Transmittance)。
(1)
式(1)中, Sample为采集到的水果原始光谱, White为白板盖放置在探头上方时获取的白参考光谱。 由于原始光谱数据中存在诸多噪声、 毛刺等干扰信号, 采用包括5点平均平滑、 归一化、 标准变量变换、 一阶导数(窗口宽度21)、 二阶导数(窗口宽度37)对光谱进行处理。
分段直接校正算法(piecewise direct standardization, PDS)是在直接校正算法基础上开发的用于模型传递的算法[11]。 采用Kennard-Stone算法从主机校正集光谱中, 分别选择5, 10, …, 75, 80个样本作为标准样进行比较。 同时考察窗口宽度(w)为3, 9, 15, 21, 31对传递结果的影响。 基于典型相关分析(canonical correlation analysis, CCA)的模型传递算法是依据CCA分析而提出的。 借助CCA可以提取两组光谱之间的线性关系, 实现光谱在主机与从机间的传递, 并消除噪声以及干扰信息的影响[12]。
本研究模型分析采用偏最小二乘算法, 并以校正集样本10折交互验证均方根误差(RMSECV)最小值来确定最佳预处理方法和最佳建模主因子数[13]。 模型的评价采用校正集相关系数(Rc)和校正均方根误差(RMSEC), 以及预测相关系数(Rp)和预测均方根误差(RMSEP)。
2 结果与讨论
2.1 实验室条件下水果糖度光谱分析
2.1.1 主机校正集光谱分析
对主机采集到的苹果、 大桃校正集光谱数据, 经过预处理算法后的PLS建模比较发现, 对于苹果采用5点平滑结合最大值归一化的预处理方式结果较好[图2(a)], 交互验证相关系数和RMSECV分别为0.885和0.628%, 最佳主因子数为9。 对于大桃采用37点的二阶导数处理方式结果较好[图2(b)], 交互验证相关系数和RMSECV分别为0.813和0.590%, 最佳主因子数为11。 将模型系数及相应的预处理算法写入检测程序以对预测集样本进行直接预测。

图 2. 经过预处理后的苹果及大桃的透射率光谱
(a): 苹果; (b): 大桃
Fig. 2. The transmittance spectra after preprocessing methods
(a): Apple; (b): Peach
2.1.2 装置预测精度验证
直接利用主机装置对预测集的样本进行预测, 采集前, 首先获取白参考光谱。 然后将预测集样本依次放置在探头上方, 点击触发按键, 即可在显示屏获取水果糖度预测值, 读数后记录。 同时, 原始光谱数据通过串口传输到电脑端保存。 待所有水果预测完成后, 采用1.4节方法, 获取预测集样本检测部位实际糖度值并记录。 检测结果如图3(a,b)所示。

图 3. 苹果和大桃糖度真实值和预测值散点图
(a): 苹果; (b)大桃
Fig. 3. Scatter plots of predicted vs . measured sugar content
(a): Apple; (b): Peach
对于苹果糖度检测, Rp和RMSEP分别为0.92和0.587%。 对比前期文献检测结果[12], 证明该装置可满足苹果糖度的快速、 有效分析。 而对大桃糖度预测, 与前期近红外光谱大桃糖度检测结果相比略差, 可能是由于在该研究中, 大桃糖度主要集中在11%~15%这一较窄范围造成预测相关系数偏低。 另外, 大桃品种的差异、 所用光谱仪的波段范围也会对检测精度产生影响。
2.1.3 主机模型到从机传递结果
图4为PDS算法传递后, 不同标准样本数量和不同窗口宽度对应的从机Rp值的变化。 从图中可以看出, 不同参数组合对Rp值的影响较大。 对于苹果糖度模型传递结果[图4(a)], 当窗口宽度为21, 标准样本数量为50时, Rp值最大为0.891, 此时对应的RMSEP为0.657%。 而对于大桃糖度模型的PDS传递结果[图4(b)], 当窗口宽度为31, 标准样本数量为65时, 此时Rp最高为0.778, RMSEP为0.725%。

图 4. PDS算法后从机R p在不同窗口宽度和标准样本数量下的变化
(a): 苹果; (b)大桃
Fig. 4. Variation of Rp obtained by piecewise direct standardization (PDS) algorithm with different numbers of transfer samples and different window sizes
(a): Apple; (b): Peach
图5为经过CCA算法传递后, 从机对预测集样本的预测结果。 对于苹果糖度模型的传递结果, 当标准样本数量为50时, 此时对应最优结果, Rp和RMSEP分别为0.883和0.641%, 如图5(a)所示, 与PDS传递结果相差不大。 而对于大桃糖度模型传递结果, 当选取45个样本作为标准样本用于传递时取得结果最好, 此时Rp和RMSEP分别为0.805和0.626%, 见图5(b)。 与PDS传递结果相比有了较大提升。 经过模型传递算法, 将主机的模型用于从机糖度预测, 结果是可行的, 虽然检测精度略有下降, 但从后续设备的批量开发, 减少建模工作量、 提升开发效率还是具有积极意义的。

图 5. 采用CCA算法后从机R p和RMSEP随不同标准样本数量的变化
(a): 苹果; (b): 大桃
Fig. 5. Variation of R p and RMSEP obtained by CCA algorithm with different numbers of transfer samples
(a): Apple; (b): Peach
2.2 树上水果糖度光谱分析
将树上采集到的水果光谱数据代入上述实验室条件下建立的模型。 图6(a,b)分别展示了使用实验室环境下构建的苹果、 大桃糖度预测模型对树上140个水果糖度的检测结果。 对大桃的检测精度与实验室条件检测结果基本一致。 对于苹果糖度的预测, 除去图中一个异常样本外, Rp提高到0.894, RMSEP下降到0.633%, 接近实验室条件下预测精度。 上述结果证明, 利用开发的检测装置及配套的遮光罩, 以及相应的光谱预处理方法, 可以实现实验室环境下构建的模型对树上水果糖度的有效检测。

图 6. 苹果和大桃糖度检测真实值和预测值散点图
(a): 苹果; (b): 大桃
Fig. 6. Scatter plots of predicted vs. measured sugar content
(a): Apple; (b): Peach
3 结论
基于微型光谱仪开发的手持式水果糖度便携式检测装置, 可用于苹果、 大桃糖度的无损、 快速分析, 在实验室环境下对苹果和大桃的预测集Rp和RMSEP分别为0.925, 0.587%和0.821, 0.613%。 相对于分段直接校正算法, 基于CCA模型传递方法, 在该样机上取得了更好的模型传递结果。 针对主机建立的用于苹果和大桃糖度预测的模型, 传递到从机后, Rp和RMSEP分别为0.883, 0.641%和0.805, 0.626%, 见图5(b)。 可以满足从机对苹果、 大桃糖度的有效检测, 实现了可见-近红外光谱糖度模型在该装置间进行共享和传递。 配合设计的遮光罩, 直接采用实验室条件下的光谱数据构建的模型预测树上水果糖度, 对苹果、 大桃糖度预测的Rp和RMSEP分别为0.866, 0.741%和0.816, 0.627%, 可以实现实验室条件下建立的模型对田间树上水果糖度的检测。
[2]
[3]
[4]
[7]
[9]
[10]
[11]
[13]
Article Outline
樊书祥, 王庆艳, 杨雨森, 李江波, 张驰, 田喜, 黄文倩. 水果糖度可见-近红外光谱手持式检测装置开发与试验[J]. 光谱学与光谱分析, 2021, 41(10): 3058. Shu-xiang FAN, Qing-yan WANG, Yu-sen YANG, Jiang-bo LI, Chi ZHANG, Xi TIAN, Wen-qian HUANG. Development and Experiment of a Handheld Visible/Near Infrared Device for Nondestructive Determination of Fruit Sugar Content[J]. Spectroscopy and Spectral Analysis, 2021, 41(10): 3058.



